Интраэпителиальная неоплазия предстательной железы высокой степени - High-grade prostatic intraepithelial neoplasia - Wikipedia
| Интраэпителиальная неоплазия предстательной железы высокой степени | |
|---|---|
| Другие имена | Простатическая интраэпителиальная неоплазия |
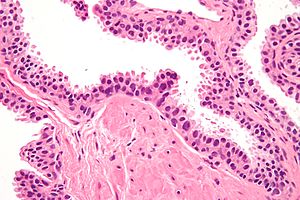 | |
| Микрофотография показывает интраэпителиальную неоплазию предстательной железы высокой степени. H&E пятно. | |
| Специальность | Урология |
Интраэпителиальная неоплазия предстательной железы высокой степени (HGPIN) является аномалией предстательной железы и, как полагают, предшествует развитию аденокарцинома простаты (наиболее распространенная форма рак простаты ).[1][2]
Его можно просто обозначить как интраэпителиальная неоплазия предстательной железы (ШТЫРЬ). Это считается предзлокачественным новообразованием или карцинома in situ простаты железы.
Признаки и симптомы
Изолированный HGPIN протекает бессимптомно. Обычно это обнаруживается при биопсии простаты, взятой для исключения рак простаты и очень часто наблюдается при удалении простаты при раке простаты.
Отношение к раку простаты
Есть несколько причин, по которым PIN является наиболее вероятным предшественником рака простаты.[3] PIN чаще встречается у мужчин с раком простаты. ПИН-код высокого уровня можно найти в 85–100% радикальная простатэктомия образцы,[4] рядом или даже в связи с раком простаты. Обычно это происходит в периферической зоне простаты. С возрастом он становится все более мультифокальным, как рак простаты. Молекулярный анализ показал, что ПИН высокой степени злокачественности и рак простаты имеют много общих генетических аномалий.[5] Это было подтверждено на модели трансгенных мышей.
Риск для мужчин с высокой степенью PIN быть диагностированным с раком простаты после повторной биопсии снизился с момента введения биопсии в более чем шести местах (традиционные биопсии секстанта).[3]
Гистология

HGPIN обычно имеет один из четырех гистологический шаблоны:[2]
- тафтинговый,
- микропапиллярный,
- крибриформ и,
- плоский.
Его цитологический особенности аденокарциномы простаты:
- присутствие ядрышки,
- повысился ядерно-цитоплазматическое соотношение и,
- повысился ядерный размер.
Микроскопически, PIN-код представляет собой набор неправильных, нетипичных эпителиальный клетки. Архитектура желез и протоков остается нормальной. Эпителиальные клетки разрастаются, и скученность приводит к псевдо-многослойный внешний вид. Они остаются полностью внутри простаты ацинус (ягодообразное окончание железы, из которой выделяется секрет) или проток. Последнее можно продемонстрировать с помощью специальных техник окрашивания (иммуногистохимия за цитокератины ) для определения базальные клетки формирующий опорный слой ацинуса. При раке простаты аномальные клетки распространяются за границы ацинуса и образуют кластеры без базальных клеток. В HGPIN базальный клеточный слой нарушен, но присутствует. PIN в основном обнаруживается в периферической зоне простаты (75-80%), редко в переходной зоне (10-15%) и очень редко в центральной зоне (5%), что соответствует зональному распределению простаты. карцинома.[6]
Потому что это считается предраковый состояние, PIN часто считается эквивалентом простаты того, что называется карцинома in situ (локализованный рак) в других органах. Однако PIN отличается от карциномы in situ тем, что может оставаться неизменным или даже спонтанно регрессировать.
Было описано несколько архитектурных вариантов PIN, и во многих случаях есть несколько шаблонов. Основные из них - пучковые, микропапиллярные, ребристые и плоские. Хотя эти различия в внешнем виде могут вызывать путаницу с другими состояниями, они не имеют клинического значения. Более редкими типами являются клетки-печатки, нейроэндокринные клетки с мелкими клетками, муцинозные, пенистые, перевернутые и с плоскоклеточной дифференцировкой.[3]
Диагностика
HGPIN диагностируется из ткани с помощью патолог, которые могут исходить из:
- игла биопсия взято через прямая кишка и,
- хирургический удаление ткани простаты:
- трансуретральная резекция простаты - удаление лишней ткани предстательной железы для улучшения мочеиспускания (лечение доброкачественная гиперплазия предстательной железы ),
- радикальная простатэктомия - полное удаление простаты и семенных пузырьков (лечение рака простаты).
Анализы крови за специфический антиген простаты (PSA), пальцевое ректальное исследование, ультразвуковое сканирование простаты через прямую кишку, тонкая игла или же медицинская визуализация исследования (такие как магнитно-резонансная томография ) находятся нет полезно для диагностики HGPIN.
Уход
Изолированный HGPIN не требует лечения. При биопсии простаты нельзя предсказать рак простаты через год, если образец простаты был хорошо взят, то есть если было 8 или более ядер.[7]
Точное время повторной биопсии остается предметом разногласий, поскольку время, необходимое для превращения HGPIN в рак простаты, и вероятность его возникновения не совсем понятны.
Прогноз
На последующем биопсия, учитывая историю HGPIN диагноз, шанс найти простатическую аденокарцинома составляет примерно 30%.[8]
История
PIN исторически подразделялся на разные стадии в зависимости от уровня клеточной атипии. PIN раньше классифицировался как PIN 1, 2 или 3, в порядке возрастания нарушений в ячейках. В настоящее время PIN 1 называется PIN низкого уровня, а PIN 2 и PIN 3 сгруппированы вместе как PIN высокого уровня.[9] Было показано, что только ПИН высокого уровня является фактором риска рака простаты. Поскольку PIN низкой степени не имеет значения и не требует повторной биопсии или лечения, он не упоминается в патология отчеты. Таким образом, ПИН-код стал синонимом ПИН-кода высокого уровня.
Смотрите также
Рекомендации
- ^ Монтирони Р., Маццучелли Р., Лопес-Бельтран А., Ченг Л., Скарпелли М. (июнь 2007 г.). «Механизмы заболевания: интраэпителиальная неоплазия предстательной железы высокой степени и другие предполагаемые пренеопластические поражения предстательной железы». Нат Клин Прак Урол. 4 (6): 321–32. Дои:10.1038 / ncpuro0815. PMID 17551536.
- ^ а б Боствик Д.Г., Цянь Дж. (Март 2004 г.). «Интраэпителиальная неоплазия предстательной железы высокой степени». Мод. Патол. 17 (3): 360–79. Дои:10.1038 / modpathol.3800053. PMID 14739906.
- ^ а б c Монтирони Р., Маццучелли Р., Лопес-Бельтран А., Ченг Л., Скарпелли М. (июнь 2007 г.). «Механизмы заболевания: интраэпителиальная неоплазия предстательной железы высокой степени и другие предполагаемые пренеопластические поражения предстательной железы». Нат Клин Прак Урол. 4 (6): 321–32. Дои:10.1038 / ncpuro0815. PMID 17551536.
- ^ Годой Г, Танежа СС (2008). «Современное клиническое ведение изолированной интраэпителиальной неоплазии предстательной железы высокой степени». Рак предстательной железы Простатический Дис. 11 (1): 20–31. Дои:10.1038 / sj.pcan.4501014. PMID 17909565.
- ^ Хьюз С., Мерфи А., Мартин С., Шейлс О., О'Лири Дж. (Июль 2005 г.). «Молекулярная патология рака простаты». J. Clin. Патол. 58 (7): 673–84. Дои:10.1136 / jcp.2002.003954. ЧВК 1770715. PMID 15976331.
- ^ Ayala, AG; Ро, JY (август 2007 г.). «Интраэпителиальная неоплазия предстательной железы: последние достижения». Архив патологии и лабораторной медицины. 131 (8): 1257–66. Дои:10.1043 / 1543-2165 (2007) 131 [1257: PINRA] 2.0.CO; 2. PMID 17683188.
- ^ Herawi, M .; Kahane, H .; Cavallo, C .; Эпштейн, JI. (Январь 2006 г.). «Риск рака простаты при первой повторной биопсии в течение 1 года после постановки диагноза интраэпителиальной неоплазии предстательной железы высокой степени связан с количеством взятых образцов». Дж Урол. 175 (1): 121–4. Дои:10.1016 / S0022-5347 (05) 00064-9. PMID 16406886.
- ^ Лейте К.Р., Камара-Лопес Л.Х., Кьюри Дж., Далл'оглио М.Ф., Санудо А., Сруги М. (июнь 2008 г.). «Обнаружение рака простаты при повторной биопсии после первоначального доброкачественного диагноза: результаты с использованием секстантной расширенной биопсии простаты». Клиники. 63 (3): 339–42. Дои:10.1590 / S1807-59322008000300009. ЧВК 2664245. PMID 18568243.
- ^ Монтирони Р., Маццучелли Р., Алгаба Ф, Лопес-Бельтран А. (сентябрь 2000 г.). «Морфологическая идентификация паттернов интраэпителиальной неоплазии предстательной железы и их значение». J. Clin. Патол. 53 (9): 655–65. Дои:10.1136 / jcp.53.9.655. ЧВК 1731241. PMID 11041054.
внешняя ссылка
| Классификация |
|---|
