Plasmodium knowlesi - Plasmodium knowlesi
| Plasmodium knowlesi | |
|---|---|
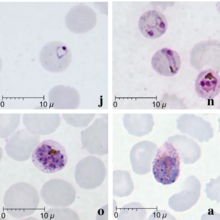 | |
| Мазки, окрашенные по Гимзе Plasmodium knowlesi заражение эритроцитов человека | |
| Научная классификация | |
| (без рейтинга): | Потогонные |
| Clade: | ЦАРЬ |
| Clade: | SAR |
| Infrakingdom: | Альвеолаты |
| Тип: | Apicomplexa |
| Учебный класс: | Aconoidasida |
| Заказ: | Гемоспориды |
| Семья: | Plasmodiidae |
| Род: | Плазмодий |
| Разновидность: | P. knowlesi |
| Биномиальное имя | |
| Plasmodium knowlesi Синтон и Маллиган 1932 | |
Plasmodium knowlesi это паразит, вызывающий малярия у человека и других приматов. Он встречается повсюду Юго-Восточная Азия, и является наиболее частой причиной малярии человека в Малайзия. Как и другие Плазмодий разновидность, P. knowlesi имеет жизненный цикл, требующий заражения как комара, так и теплокровного хозяина. А естественные теплокровные хозяева P. knowlesi вероятно, разные Обезьяны Старого Света, люди могут быть инфицированы P. knowlesi если они питаются инфицированными комарами. P. knowlesi эукариот в типе Apicomplexa, род Плазмодий, и подрод Плазмодий. Наиболее тесно связан с паразитом человека. Плазмодий вивакс а также другие Плазмодий виды, которые заражают нечеловеческих приматов.
Люди инфицированы P. knowlesi может развиваться несложный или же тяжелая малярия аналогично тому, что вызвано Плазмодий falciparum. Диагностика P. knowlesi инфекция является сложной задачей, поскольку P. knowlesi очень похож на другие виды, заражающие людей. Лечение аналогично другим видам малярии, с хлорохин или же комбинированная терапия артемизинином обычно рекомендуется. P. knowlesi малярия - это развивающееся заболевание, которое ранее считалось редким для людей, но все чаще признается серьезным бременем для здоровья в Юго-Восточной Азии.
P. knowlesi был впервые описан как отдельный вид и как потенциальная причина малярии у человека в 1932 году. В начале 20 века его ненадолго использовали, чтобы вызвать лихорадку в качестве лечения нейросифилис. В середине 20 века P. knowlesi стал популярным как инструмент для изучения Плазмодий биологии и использовался для фундаментальных исследований, исследований вакцин и разработки лекарств. P. knowlesi до сих пор используется в качестве лабораторной модели малярии, так как легко поражает модель примат макака резус, и его можно выращивать в культура клеток в крови человека или макаки.
Жизненный цикл

Как и другие Плазмодий паразиты, P. knowlesi имеет жизненный цикл, который требует, чтобы он передавался туда и обратно между хозяевами-млекопитающими и хозяевами-насекомыми. Приматы заражаются через укус зараженного Анофелес комар, переносящий стадию паразита, называемую спорозоит в его слюнных железах. Спорозоиты следуют по кровотоку к печени приматов, где они развиваются и размножаются в течение пяти-шести дней, прежде чем взорваться, высвобождая тысячи дочерних клеток, называемых мерозоиты в кровь (в отличие от родственных P. vivax, P. knowlesi не делает скрытого гипнозоиты в печени).[1][2] Мерозоиты в крови прикрепляются к приматам и вторгаются в них. красные кровяные тельца. Внутри эритроцита паразит проходит несколько морфологически различимых стадий, называемых стадией кольца, трофозоитом и шизонтом. Зараженные шизонтом эритроциты в конечном итоге лопаются, высвобождая до 16 новых мерозоитов в кровоток, которые инфицируют новые эритроциты и продолжают цикл.[1][3] P. knowlesi завершает этот цикл эритроцитов каждые 24 часа, что делает его исключительно быстрым среди заражающих приматов Плазмодий виды (обычно это занимает 48 или 72 часа).[2] Иногда паразиты, которые вторгаются в эритроциты, вместо этого вступают в половой цикл, развиваясь примерно за 48 часов в отдельные половые формы, называемые микрогаметоцитами или макрогаметоцитами.[1][3] Эти гаметоциты остаются в крови, чтобы их могли проглотить комары.[1][3]
Комар заглатывает гаметоциты, когда принимает кровяная мука от зараженного хозяина приматов. Попав внутрь кишечника комара, гаметоциты развиваются в гаметы а затем слиться, чтобы сформировать диплоид зигота.[1] Зигота превращается в оокинете, который мигрирует через стенку кишки комара и превращается в ооциста.[1][4] Затем ооциста выделяет тысячи спорозоитов, которые мигрируют через комаров в слюнные железы.[1] Весь этот процесс у комара занимает от 12 до 15 дней.[2]
Клеточная биология

P. knowlesi во многом напоминает другие Плазмодий разновидность в своей клеточной биологии. Его геном состоит из 23,5 мегабазы ДНК разделены на 14 хромосомы.[5] Он содержит около 5200 генов, кодирующих белок, 80% из которых имеют ортологи присутствует в P. falciparum и P. vivax.[5] Геном содержит два больших семейства генов, уникальных для P. knowlesi: семейство SICAvar (вариант агглютинации клеток, инфицированных шизонтом), которое участвует в отображении различных антигены на поверхности паразита, чтобы ускользнуть от иммунной системы, и семейство Kir (knowlesi interspersed repeat), участвующих в прикреплении паразитирующих эритроцитов к стенкам кровеносных сосудов.[5]
Как апикомплекс, P. knowlesi имеет несколько отличительных структур на своей апикальный конец которые специализируются на проникновении в клетки-хозяева. К ним относятся большие луковичные Rhoptries, меньше микронемы, и разошлись плотные гранулы, каждый из которых секретирует эффекторы для проникновения и модификации клетки-хозяина.[6][7] Как и другие апикомплексаны, P. knowlesi также есть два органеллы из эндосимбиотическое происхождение: один большой митохондрия и апикопласт, оба из которых участвуют в метаболизм.[8]
Эволюция и таксономия
Несмотря на морфологическое сходство с P. malariae, P. knowlesi наиболее тесно связан с P. vivax а также другие Плазмодий виды, которые заражают нечеловеческих приматов.[9] Последний общий предок всех современных P. knowlesi штаммы жили приблизительно от 98000 до 478000 лет назад.[9] Среди человеческих паразитов, P. knowlesi наиболее тесно связан с P. vivax, от которого он отклонился между 18 и 34 миллионами лет назад.[5][10] А филогенетическое дерево сравнивая Плазмодий виды, заражающие людей, показаны ниже:[5]
| ПодродПлазмодий |
| ||||||||||||||||||
Население P. knowlesi паразиты более генетически разнообразны, чем паразиты P. falciparum или же P. vivax. В P. knowlesi Есть три генетически различных субпопуляции.[5] Два из них обитают в одних и тех же районах Малайзийского Борнео и могут заражать разных комаров.[5] Третий был обнаружен только в лабораторных изолятах, происходящих из других частей Юго-Восточной Азии.[5] Популяции P. knowlesi изолированные от макак генетически неотличимы от тех, которые изолированы от инфекций человека, что позволяет предположить, что одни и те же популяции паразитов могут инфицировать людей и макак взаимозаменяемо.[11]
Три подвида P. knowlesi были описаны на основании различий в их внешнем виде в окрашенных мазках крови: P. knowlesi edesoni, P. knowlesi sintoni, и P. knowlesi arimai, которые были изолированы от Малайзии, Ява, и Тайвань соответственно.[2][12] Отношения между этими описанными подвидами и популяциями, описанными в современной литературе, не ясны.[2]
Распределение
Plasmodium knowlesi находится повсюду Юго-Восточная Азия, где он в первую очередь поражает длиннохвостая макака, коснохвостая макака, и Суматранский сурили а также комары-переносчики Anopheles hackeri в полуостровной Малайзии и Анофелес латенс в Саравак.[1] Длиннохвостые макаки в дикой природе могут быть заражены P. knowlesi без каких-либо явных заболеваний, даже если они одновременно инфицированы различными другими Плазмодий разновидность.[2][10] P. knowlesi редко встречается за пределами Юго-Восточной Азии, вероятно, потому что комары, которых он заражает, обитают только в этом регионе.[11]
Роль в заболевании человека

P. knowlesi может вызвать оба несложный и суровый малярия у людей. Зараженные почти всегда испытывают высокая температура и озноб.[13] Людям с несложным P. knowlesi при малярии также часто возникают головные боли, боли в суставах, недомогание и потеря аппетита.[13] Реже люди сообщают о кашле, боли в животе, диарее, тошноте и рвоте.[13] Лабораторные тесты инфицированных людей почти всегда показывают низкое количество тромбоцитов, хотя это редко приводит к кровотечениям.[13] В отличие от других человеческих малярий, P. knowlesi малярия, как правило, имеет лихорадку, которая повышается каждые 24 часа, и поэтому ее часто называют ежедневной или «повседневной» малярией.[13][14] Несложный P. knowlesi малярию можно лечить противомалярийные препараты.[13]
Не менее 10% людей инфицированы P. knowlesi заболеть тяжелой малярией.[11] Суровый P. knowlesi малярия похожа на тяжелую малярию, вызванную P. falciparum. Люди с тяжелым заболеванием могут испытывать одышку, боль в животе и рвоту.[13] По мере прогрессирования болезни паразиты размножаются очень высокие уровни в крови может вызвать острое повреждение почек, желтуха, шок и респираторный дистресс.[13][15] Метаболический ацидоз встречается редко, но может возникнуть в особо тяжелых случаях.[15] В отличие от P. falciparum малярия, тяжелая форма P. knowlesi малярия редко вызывает кома или серьезный анемия.[13][15] Примерно 1-2% случаев заканчиваются летальным исходом.[11]
Диагностика
Малярия традиционно диагностируется путем обследования Окрашенный по Гимзе мазки крови под микроскопом; однако, дифференцируя P. knowlesi От других Плазмодий виды таким образом являются сложными из-за их схожего внешнего вида.[11] P. knowlesi кольцевые паразиты, окрашенные Гимзой, напоминают P. falciparum этапы кольца, представляющие собой круг с одной или двумя темными точками хроматин.[16] Более старые трофозоиты кажутся более рассредоточенными, образуя прямоугольную форму, распределенную по клетке-хозяину, называемую «полосообразной формой», которая напоминает аналогичную стадию в P. malariae.[16] Во время этой стадии на эритроците хозяина иногда появляются точки, что называется «пунктирная линия Синтона и Маллиганса».[16] Появляются шизонты, как и другие Плазмодий видов, как скопления пурпурных мерозоитов, окружающих центральный пигмент темного цвета.[16]
Из-за морфологического сходства среди Плазмодий виды, неправильный диагноз P. knowlesi инфекция как P. falciparum, P. malariae, или же P. vivax обычное дело.[15] Хотя некоторые экспресс-тесты может обнаружить P. knowlesi, они, как правило, плохо чувствительность и специфичность и поэтому не всегда надежны.[15][17] Обнаружение нуклеиновая кислота к ПЦР или же ПЦР в реальном времени это самый надежный метод обнаружения P. knowlesi, и отличая его от других Плазмодий видовая инфекция. Однако из-за относительно медленного и дорогостоящего характера ПЦР она недоступна во многих эндемичных районах.[11] Петлевая изотермическая амплификация методы P. knowlesi обнаружения также были разработаны, но пока не получили широкого распространения.[11]
Уход
Потому что P. knowlesi Для завершения эритроцитарного цикла требуется всего 24 часа, это может быстро привести к очень высокому уровню паразитемии с фатальными последствиями.[15] Для тех, у кого неосложненная малярия, то Всемирная организация здоровья рекомендует лечение с комбинированная терапия на основе артемизинина (Актер хлорохин.[18] Для тех, у кого тяжелая малярия, Всемирная организация здравоохранения рекомендует введение внутривенного артесунат в течение как минимум 24 часов с последующим лечением АКТ.[15] Кроме того, ранние испытания лекарств показали, что комбинации хлорохина и примахин, артесунат и мефлохин, артеметер и люмефантрин, и один хлорохин может быть эффективным лечением неосложненных P. knowlesi малярия.[15] Нет никаких доказательств P. knowlesi развитие устойчивости к текущим противомалярийным препаратам.[15]
Эпидемиология
P. knowlesi является наиболее частой причиной малярии в Малайзия,[5] и случаи P. knowlesi малярия была зарегистрирована в большинстве стран Юго-Восточной Азии, а также у путешественников из этого региона.[11]
Заражение P. knowlesi связано с социально-экономическими факторами и факторами образа жизни, которые приводят людей в густые леса, где обычно встречаются хозяева комаров.[13] В частности, повышенному риску заражения подвержены те, кто работает в лесу или на его окраинах, например, фермеры, охотники и лесорубы.[13] Вероятно, по этой причине мужчины заражаются чаще, чем женщины, а взрослые заражаются чаще, чем дети.[13]
Исследование
P. knowlesi долгое время использовалась в качестве исследовательской модели для изучения взаимодействия между паразитом и хозяином, а также для разработки противомалярийных вакцин и лекарств.[10] Его полезность в качестве исследовательской модели частично объясняется его способностью заражать макак-резус, обычных лабораторных модельных приматов. Макаки-резус очень восприимчивы к P. knowlesi и может быть заражен укусом комара, инъекцией спорозоитов или инъекцией паразитов на стадии крови.[2][10] У инфицированных обезьян появляются некоторые признаки малярии человека, включая анемию и увеличение селезенки и печени.[2] Инфекция, как правило, приводит к летальному исходу, если ее не лечить, причем причина смерти кровообращение отказ, характеризующийся адгезией инфицированных эритроцитов к кровеносный сосуд стены.[2] Обезьян можно вылечить от инфекции путем лечения противомалярийными средствами; повторное заражение с последующим излечением приводит к тому, что у обезьян развивается некоторый иммунитет к инфекции, эта тема также была предметом серьезных исследований.[2]
P. knowlesi также используется для in vitro исследования в Плазмодий клеточная биология. Изолированные спорозоиты могут инфицировать начальный резус гепатоциты, позволяя in vitro исследование паразитарной стадии печени.[10] Кроме того, P. knowlesi и P. falciparum единственные Плазмодий виды, которые могут постоянно поддерживаться в культурный красные кровяные тельца, как резус, так и человеческие.[10] Содействуя исследованиям в области молекулярной биологии, P. knowlesi геном секвенирован и доступен на PlasmoDB и другие онлайн-репозитории.[10] P. knowlesi могут быть генетически модифицированы в лаборатории трансфекция либо в модельной системе макаки-резуса, либо в культуре клеток крови.[10][19] Стадии заражения крови и спорозоиты могут храниться длительное время путем замораживания глицерин, позволяя сохранить интересующие штаммы.[1]
История

Итальянский врач Джузеппе Франкини сначала описал, что могло быть P. knowlesi в 1927 году, когда он заметил паразита, отличного от P. cynomolgi и П. инуи в крови длиннохвостой макаки.[20][21] В 1931 году Х. М. Кэмпбелл снова заметил паразита у длиннохвостой макаки во время его работы над кала азар (висцеральный лейшманиоз ) в Калькутта; Коллега Кэмпбелла Лайонел Эверард Напье взял кровь у пораженной обезьяны и привитый три лабораторных обезьяны, одна из которых была макакой-резус, у которой развилась тяжелая инфекция.[3][22] Кэмпбелл и Напье передали зараженную обезьяну Бирадж Мохан Дас Гупта кто смог сохранить паразита путем последовательного прохождения через обезьян.[23] В 1932 году Дас Гупта и его руководитель Роберт Ноулз описал морфологию паразита в крови макака и продемонстрировал, что он может заразить трех пациентов-людей (в каждом случае он использовался, чтобы вызвать лихорадку с надеждой вылечить другую инфекцию).[3][24] Также в 1932 г. Джон Синтон и Х. В. Маллиган далее описали морфологию паразита в клетках крови, определили, что это особый вид от других описанных, и назвали его Plasmodium knowlesi в честь Роберта Ноулза.[3]
Вскоре после этого, в 1935 г. К. Э. Ван Ройен и Джордж Р. Пайл сообщили об использовании P. knowlesi инфекция лечить общий паралич у психиатрических больных. P. knowlesi будет использоваться в качестве генерала пиретический агент при различных заболеваниях, в частности нейросифилис для которого он использовался как минимум до 1955 года.[23] Пока Сирил Гарнхэм предложил в 1957 г. P. knowlesi может естественным образом заразить людей,[25] первый задокументированный случай естественного заражения человека P. knowlesi В 1965 году он находился в полицейском участке армии США, у которого после пятидневной службы в Малайзии начался озноб и жар.[23][26] Основываясь на этом открытии, группа из Института медицинских исследований полуострова Малайзия провела опрос людей, живущих в непосредственной близости от макак, но не смогла найти доказательств того, что обезьянья малярия передается человеку.[23]
В 1960-х и 1970-х годах научно-исследовательские группы использовали P. knowlesi в качестве модели исследования, чтобы сделать важные открытия в области малярии. В 1965 и 1972 годах несколько групп описали, как P. knowlesi антигенная вариация способствовал уклонению от иммунитета и хронической инфекции.[23] В 1975 г. Луи Х. Миллер и другие показали, что P. knowlesi требуется Фактор Даффи на поверхности красных кровяных телец, чтобы вторгнуться в них (они будут демонстрировать то же требование для P. vivax год спустя).[23]
Работа над P. knowlesi как паразит малярии человека возродился в 2004 г., когда Бальбир Сингх и другие использовали ПЦР чтобы показать, что более половины группы людей с диагнозом P. malariae малярии на Малайзийском Борнео были фактически инфицированы P. knowlesi.[23][27] В течение следующего десятилетия несколько исследователей использовали методы молекулярного обнаружения, способные различать P. knowlesi от морфологически похожих паразитов, чтобы связать растущую долю случаев малярии с P. knowlesi по всей Юго-Восточной Азии.[28] Работа с архивными образцами показала, что заражение этим паразитом происходило в Малайзии как минимум с 1990-х годов.[29]
Рекомендации
- ^ а б c d е ж грамм час я Коллинз В.Е. (2012). "Plasmodium knowlesi: малярийный паразит обезьян и людей". Ежегодный обзор энтомологии (Представлена рукопись). 57: 107–121. Дои:10.1146 / annurev-ento-121510-133540. PMID 22149265.
- ^ а б c d е ж грамм час я j Бутчер Г.А., Митчелл Г.Х. (сентябрь 2016 г.). "Роль Plasmodium knowlesi в истории исследований малярии ». Паразитология. Издательство Кембриджского университета. 145 (1): 6–17. Дои:10.1017 / S0031182016001888. PMID 27829470.
- ^ а б c d е ж Коатни Г.Р., Коллинз В.Е., Уоррен М., Контакос П.Г. (1971). Примат Маларий. Атланта, Джорджия: Отдел паразитарных болезней, Центры контроля заболеваний США. стр. 317–334. Получено 26 августа 2019.
- ^ Смит Р.К., Бариллас-Мюри С. (декабрь 2016 г.). "Плазмодий Ооцисты: недооцененные мишени иммунитета от комаров ». Тенденции в паразитологии. Эльзевир. 32 (12): 979–990. Дои:10.1016 / j.pt.2016.08.012. PMID 27639778.
- ^ а б c d е ж грамм час я Гарридо-Карденас Дж. А., Гонсалес-Серон Л., Мансано-Агульяро Ф, Меса-Валле С. (январь 2019 г.). "Плазмодий геномика: подход к изучению малярии человека и борьбе с ней ». Паразитологические исследования. Springer. 118 (1): 1–27. Дои:10.1007 / s00436-018-6127-9. PMID 30402656. S2CID 53228888.
- ^ Кунихан, Натали А .; Каланон, Мин; Коппель, Росс Л .; Де Конинг-Уорд, Таня Ф. (2013). «Белки Plasmodium rhoptry: Почему важен порядок». Тенденции в паразитологии. 29 (5): 228–36. Дои:10.1016 / июл.2013.03.003. PMID 23570755.
- ^ Кемп, Луиза Э .; Ямамото, Масахиро; Солдати-Фавр, Доминик (2013). «Подрыв клеточных функций хозяина апикомплексными паразитами». Обзор микробиологии FEMS. 37 (4): 607–31. Дои:10.1111/1574-6976.12013. PMID 23186105.
- ^ Шейнер, Лилач; Вайдья, Ахил Б .; Макфадден, Джеффри И. (2013). «Метаболическая роль эндосимбиотических органелл Toxoplasma и Plasmodium spp». Текущее мнение в микробиологии. 16 (4): 452–8. Дои:10.1016 / j.mib.2013.07.003. ЧВК 3767399. PMID 23927894.
- ^ а б Ли К.С., Divis PC, Закария СК, Матусоп А., Джулин Р.А., Конвей Д.Д., Кокс-Сингх Дж., Сингх Б. (2011). Казура JW (ред.). "Plasmodium knowlesi: резервуары-хозяева и отслеживание появления у людей и макак". PLOS Pathog. 7 (4): e1002015. Дои:10.1371 / journal.ppat.1002015. ЧВК 3072369. PMID 21490952.
- ^ а б c d е ж грамм час Pasini EM, Zeeman AM, Voorberg-Vanderwel A, Kocken CH (ноябрь 2016 г.). "Plasmodium knowlesi: актуальная универсальная экспериментальная модель малярии ". Паразитология. Издательство Кембриджского университета. 145 (1): 56–70. Дои:10.1017 / S0031182016002286. PMID 27938428.
- ^ а б c d е ж грамм час Миллар С.Б., Кокс-Сингх Дж. (Июль 2015 г.). "Человеческие инфекции с Plasmodium knowlesi-зоонозная малярия ». Клиническая микробиология и инфекции. Эльзевир. 21 (7): 640–648. Дои:10.1016 / j.cmi.2015.03.017. PMID 25843504.
- ^ Гарнхэм ПК (1963). «Новый подвид Plasmodium knowlesi у длиннохвостой макаки». J Trop Med Hyg. 66: 156–8. PMID 13960457.
- ^ а б c d е ж грамм час я j k л Сингх Б., Данешвар С. (2013). «Инфекции человека и обнаружение Plasmodium knowlesi». Обзоры клинической микробиологии. 26 (2): 165–184. Дои:10.1128 / CMR.00079-12. ЧВК 3623376. PMID 23554413.
- ^ Чин В., Контакос П.Г., Коатни Р.Г., Кимбал Х.Р. (1965). «Естественно приобретенная банальная малярия у человека, передаваемая обезьянам». Наука. 149 (3686): 865. Bibcode:1965 г., наука ... 149..865C. Дои:10.1126 / science.149.3686.865. PMID 14332847. S2CID 27841173.
- ^ а б c d е ж грамм час я Барбер Б.Е., Григг М.Дж., Уильям Т., Йео Т.В., Ансти Н.М. (март 2017 г.). "Лечение Plasmodium knowlesi малярия ». Тенденции в паразитологии. Эльзевир. 33 (3): 242–253. Дои:10.1016 / j.pt.2016.09.002. PMID 27707609.
- ^ а б c d "DPDx Malaria - Галерея изображений". Центры США по контролю и профилактике заболеваний. 29 декабря 2017 г.. Получено 20 января 2020.
- ^ Despommier DD, Гриффин Д.О., Gwadz RW, Hotez PJ, Knirsch CA. Паразитарные болезни (PDF) (7-е изд.). Паразиты без границ. п. 112.
- ^ "Лечение неосложненной малярии, вызванной P. vivax, P. ovale, P. malariae, или же P. knowlesi". Рекомендации по лечению малярии (3-е изд.). Всемирная организация здоровья. 2015. стр. 60. ISBN 978-92-4-154912-7. Получено 22 января 2020.
- ^ де Конинг-Уорд TF; Gilson PR; Crabb BS (июнь 2015 г.). «Достижения молекулярно-генетических систем при малярии». Обзоры природы Микробиология. Макмиллан. 13 (6): 373–387. Дои:10.1038 / nrmicro3450. PMID 25978707. S2CID 19786233.
- ^ Franchini G (1927) Su di un plasmodio pigmentato di una scimmia. Arch Ital Sci Med Colon 8: 187–90
- ^ Антинори С., Милаццо Л., Корбеллино М. (октябрь 2011 г.). "Plasmodium knowlesi: забытое итальянское открытие? ". Клинические инфекционные болезни. 53 (8): 849, ответ автора 849–50. Дои:10.1093 / cid / cir527. PMID 21890752.
- ^ Napier LE; Кэмпбелл HGM (май 1932 г.). «Наблюдения за инфекцией Plasmodium, которая вызывает гемоглобинурию у некоторых видов обезьян» (PDF). Индийский медицинский вестник: 246–249. S2CID 26553543. Получено 27 августа 2019.
- ^ а б c d е ж грамм Спинелло А, Галимберти Л., Милаазо Л., Корбеллино М. (2013). «Plasmodium knowlesi: появляющийся зоонозный паразит малярии». Acta Tropica. 125 (2): 191–201. Дои:10.1016 / j.actatropica.2012.10.008. PMID 23088834.
- ^ Ноулз Р., Дас Гупта Б.М. (июнь 1932 г.). «Исследование обезьяньей малярии и ее экспериментальной передачи человеку». Индийский медицинский вестник. 67 (6): 301–320. ЧВК 5231565. PMID 29010910.
- ^ Гарнем П.К., Лейнсон Р., Купер В. (1957). «Тканевые стадии и спорогония Plasmodium knowlesi". Транс Р Соц Троп Мед Хиг. 51 (5): 384–396. Дои:10.1016/0035-9203(57)90071-8. PMID 13467997.
- ^ Мейсон Дентинджер, Р. (26 августа 2015 г.). "Паттерны заражения и закономерности эволюции: как малярийный паразит сблизил" обезьян и человека в 1960-е годы ". Журнал истории биологии. 49 (2): 359–395. Дои:10.1007 / s10739-015-9421-8. PMID 26307748.
- ^ Сингх Б., Ли К.С., Матусоп А., Радхакришнан А., Шамсул С.С., Кокс-Сингх Дж., Томас А., Конвей Д. Д. (2004). "Большое внимание естественно приобретенным Plasmodium knowlesi инфекции у людей " (PDF). Ланцет. 363 (9414): 1017–24. Дои:10.1016 / S0140-6736 (04) 15836-4. PMID 15051281. S2CID 7776536.
- ^ Vythilingam I, Noorazian YM, Huat TC, Jiram AI, Yusri YM, Azahari AH, Norparina I, Noorrain A, Lokmanhakim S (2008). «Plasmodium knowlesi у людей, макак и комаров на полуострове Малайзия». Векторы паразитов. 1 (1): 26. Дои:10.1186/1756-3305-1-26. ЧВК 2531168. PMID 18710577.
- ^ Ли К.С.; Кокс-Сингх Дж; Brooke G; Матусоп А; Сингх Б. (2009). «Plasmodium knowlesi из архивных мазков крови: еще одно свидетельство того, что человеческие инфекции широко распространены и не возникают вновь на Малайзийском Борнео». Int J Parasitol. 39 (10): 1125–1128. Дои:10.1016 / j.ijpara.2009.03.003. ЧВК 2722692. PMID 19358848.
внешняя ссылка
- Страница CDC по малярии
- Страница ВОЗ по малярии
- Данные о геноме P. knowlesi
- Короткометражный фильм об открытии роли P. knowlesi при малярии человека
| Схолия имеет тема профиль для Plasmodium knowlesi. |
