Атеросклероз - Atherosclerosis
| Атеросклероз | |
|---|---|
| Другие имена | Артериосклеротическое заболевание сосудов (АСЗС) |
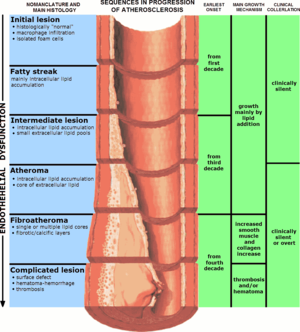 | |
| Прогрессирование атеросклероза (сужение преувеличено) | |
| Специальность | Кардиология, ангиология |
| Симптомы | Никто[1] |
| Осложнения | Ишемическая болезнь сердца, Инсульт, заболевание периферических артерий, проблемы с почками[1] |
| Обычное начало | Молодость (ухудшается с возрастом)[2] |
| Причины | Неизвестный[1] |
| Факторы риска | Высокое кровяное давление, сахарный диабет, курение, ожирение, семейный анамнез, нездоровое питание[3] |
| Профилактика | Здоровая диета, упражнения, отказ от курения, поддержание нормального веса[4] |
| Медикамент | Статины, лекарства от кровяного давления, аспирин[5] |
| Частота | ≈100% (> 65 лет)[6] |
Атеросклероз заболевание, при котором стенка артерия развиваются аномалии, называемые высыпаниями. Эти поражения могут привести к сужению из-за накопления атероматозный налет.[7] Вначале симптомы вообще отсутствуют.[1] В тяжелых случаях это может привести к ишемическая болезнь сердца, Инсульт, заболевание периферических артерий, или же проблемы с почками, в зависимости от того, какие артерии поражены.[1] Симптомы, если они возникают, обычно проявляются не раньше среднего возраста.[3]
Точная причина неизвестна.[1] Факторы риска включают: аномальный уровень холестерина, повышенный уровень воспалительные маркеры,[8] высокое кровяное давление, сахарный диабет, курение, ожирение, семейный анамнез и нездоровое питание.[3] Зубной налет состоит из жира, холестерин, кальций, и другие вещества, обнаруженные в кровь.[7] Сужение артерий ограничивает приток богатой кислородом крови к частям тела.[7] Диагноз основывается на физическом осмотре, ЭКГ, и тест с физической нагрузкой, среди прочего.[9]
Профилактика обычно заключается в употреблении в пищу Здоровая диета, заниматься спортом, не курить и поддерживать нормальный вес.[4] Лечение установленного заболевания может включать лекарства для снижения уровня холестерина, такие как статины, лекарства от кровяного давления или лекарства, снижающие свертываемость, например аспирин.[5] Также может быть проведен ряд процедур, таких как чрезкожное коронарное вмешательство, шунтирование коронарной артерии, или же каротидная эндартерэктомия.[5]
Атеросклероз обычно начинается в молодом возрасте и с возрастом ухудшается.[2] Почти все люди в той или иной степени страдают к 65 годам.[6] Это номер один причина смерти и инвалидность в разработанный мир.[10] Хотя впервые он был описан в 1575 году,[11] есть свидетельства того, что это заболевание возникло у людей более 5000 лет назад.[11]
Определения
Следующие термины похожи, но различаются как по написанию, так и по значению, и их легко спутать: атеросклероз, артериолосклероз, и атеросклероз. Артериосклероз - общий термин, описывающий любое затвердевание (и потерю эластичности) средних или крупных артерий (от Греческий ἀρτηρία (artēria) 'артерия' и σκλήρωσις (склероз ) 'закалка'); артериолосклероз есть ли какое-либо затвердевание (и потеря эластичности) артериолы (мелкие артерии); атеросклероз затвердение артерии именно из-за атероматозной бляшки (от Древнегреческий ἀθήρα (Athḗra) 'каша'). Период, термин атерогенный используется для веществ или процессов, вызывающих образование атерома.[12]
Признаки и симптомы
Атеросклероз протекает бессимптомно в течение десятилетий, потому что артерии увеличиваются во всех местах расположения бляшек, и это не влияет на кровоток.[13] Даже большинство разрывы бляшек не вызывают симптомов до тех пор, пока не произойдет достаточное сужение или закрытие артерии из-за тромбов. Признаки и симптомы возникают только после того, как сильное сужение или закрытие препятствует притоку крови к различным органам, достаточному для возникновения симптомов.[14] В большинстве случаев пациенты осознают, что у них болезнь, только когда они испытывают другие сердечно-сосудистые заболевания такие как инсульт или сердечный приступ. Однако эти симптомы все еще различаются в зависимости от пораженной артерии или органа.[15]
Аномалии, связанные с атеросклерозом, начинаются в детстве. Фиброзные и студенистые поражения наблюдались в коронарных артериях у детей 6-10 лет.[16] Жирные полосы наблюдались в коронарных артериях у подростков 11-15 лет,[16] хотя они появляются в гораздо более молодом возрасте в аорте.[17]
Клинически, учитывая увеличение артерий в течение десятилетий, симптоматический атеросклероз обычно встречается у мужчин в возрасте 40 лет и женщин в возрасте от 50 до 60 лет. Субклинически заболевание начинает проявляться в детстве и редко проявляется уже при рождении. Заметные признаки могут появиться в период полового созревания. Хотя симптомы редко проявляются у детей, раннее обследование детей на сердечно-сосудистые заболевания может быть полезным как для ребенка, так и для его / ее родственников.[18] В то время как ишемическая болезнь сердца чаще встречается у мужчин, чем у женщин, атеросклероз церебральных артерий и инсульты одинаково поражают оба пола.[19]
Заметное сужение в коронарных артериях, которые несут ответственность за доставку насыщенной кислородом крови к сердцу, могут вызывать такие симптомы, как боль в груди, стенокардия и одышка, потливость, тошнота, головокружение или бред, одышка или сердцебиение.[15] Аномальные сердечные ритмы, называемые аритмиями, когда сердце бьется слишком медленно или слишком быстро, являются еще одним следствием ишемия.[20]
Сонные артерии снабжают кровью мозг и шею.[20] Заметное сужение сонных артерий может проявляться такими симптомами, как чувство слабости, неспособность думать ровно, трудности с речью, головокружение и трудности при ходьбе или вставании прямо, нечеткость зрения, онемение лица, рук и ног. , сильная головная боль и потеря сознания. Эти симптомы также связаны с инсультом (смертью клеток мозга). Инсульт вызывается выраженным сужением или закрытием артерий, идущих к мозгу; отсутствие адекватного кровоснабжения приводит к гибели клеток пораженной ткани.[21]
Периферические артерии, которые снабжают кровью ноги, руки и таз, также испытывают заметное сужение из-за разрыва бляшек и образования тромбов. Симптомами заметного сужения являются онемение рук или ног, а также боль. Еще одним важным местом образования бляшек являются почечные артерии, кровоснабжающие почки. Возникновение и накопление налета приводит к снижению кровотока в почках и хроническому заболеванию почек, которое, как и все другие области, обычно бессимптомно до поздних стадий.[15]
По данным США на 2004 год, примерно у 66% мужчин и 47% женщин первый симптом атеросклероза сердечно-сосудистые заболевания это острое сердечно-сосудистое заболевание или же внезапная сердечная смерть (смерть в течение одного часа после появления симптома).Сердечное стресс-тестирование, традиционно наиболее часто применяемый неинвазивный метод тестирования ограничений кровотока, как правило, выявляет только просвет сужение ≈75% или больше, хотя некоторые врачи утверждают, что методы ядерного стресса могут обнаружить лишь 50%.
Тематические исследования включали вскрытие трупов солдат США, погибших в Вторая Мировая Война и Корейская война. Часто цитируемый отчет включал вскрытие трупов 300 американских солдат, убитых в Корее. Хотя средний возраст мужчин составлял 22,1 года, 77,3% имели «явные признаки коронарного артериосклероза».[22] Другие исследования солдат в война во Вьетнаме показали аналогичные результаты, хотя часто хуже, чем результаты предыдущих войн. Теории включают высокие показатели употребление табака и (в случае с вьетнамскими солдатами) появление обработанных пищевых продуктов после Второй мировой войны.
Факторы риска

Атеросклеротический процесс изучен недостаточно. Атеросклероз связан с воспалительными процессами в эндотелиальных клетках стенки сосуда, связанными с сохраненными липопротеин низкой плотности (ЛПНП) частицы.[23] Эта задержка может быть причиной, следствием или и тем, и другим основного воспалительного процесса.[24]
Присутствие бляшки заставляет мышечные клетки кровеносного сосуда растягиваться, компенсируя дополнительный объем, а эндотелиальная выстилка утолщается, увеличивая разделение между бляшкой и просветом. Это несколько компенсирует сужение, вызванное ростом бляшки, но заставляет стенку становиться жестче и становиться менее податливой для растяжения с каждым ударом сердца.[25]
Изменяемый
- Бактериальные инфекции[26]
- Сахарный диабет[27]
- Дислипидемия[27]
- Курение табака[27]
- Транс-жиры[27]
- Абдоминальное ожирение[27]
- Диета по западному образцу[27]
- Резистентность к инсулину[27]
- Гипертония[27]
- ВИЧ / СПИД[28]
Немодифицируемый
- Пожилой возраст[27][29]
- Мужской[27]
- Генетические аномалии[27]
- История семьи[27]
- Коронарная анатомия и паттерн ветвей[30]
Меньший или неопределенный
- Южная Азия спуск[31][32]
- Тромбофилия[33][34][35]
- Насыщенный жир[27][36]
- Излишний углеводы[27][37]
- Повышенный триглицериды[27]
- Системное воспаление[38]
- Гиперинсулинемия[39]
- Недосыпание[40]
- Загрязнение воздуха[41][42]
- Сидячий образ жизни[27]
- Отравление мышьяком[43]
- Алкоголь[27]
- Хронический стресс[27]
- Гипотиреоз[44]
- Парадантоз[45]
Диетический
Связь между диетическим жиром и атеросклерозом противоречива. Писать в Наука, Гэри Таубс уточнил, что политические соображения сыграли роль в рекомендациях государственных органов.[46] В USDA, в его пищевая пирамида, продвигает диету, состоящую из примерно 64% углеводов от общего количества калорий. В Американская Ассоциация Сердца, то Американская диабетическая ассоциация и Национальная образовательная программа по холестерину дать аналогичные рекомендации. Напротив, проф. Уолтер Уиллетт (Гарвардская школа общественного здравоохранения, ЧИСЛО ПИ второй Исследование здоровья медсестер ) рекомендует гораздо более высокий уровень жира, особенно мононенасыщенный и полиненасыщенные жиры.[47] Однако эти диетические рекомендации достигли консенсуса в отношении отказа от потребления транс-жиры.
Роль поедания окисленных жиров (прогорклые жиры ) у людей неясно. У кроликов, которых кормили прогорклыми жирами, быстрее развивается атеросклероз.[48] Крыс накормили DHA -содержащие масла испытали заметные нарушения их антиоксидант систем и накопили значительное количество фосфолипид гидропероксид в их крови, печени и почках.[49]
Было обнаружено, что кролики, получавшие атерогенную диету, содержащую различные масла, подвергаются наибольшей окислительной восприимчивости ЛПНП через полиненасыщенные масла.[50] В другом исследовании кроликов, получавших нагретое соевое масло, «гистологически и клинически продемонстрировали сильно индуцированный атеросклероз и выраженное повреждение печени».[51] Тем не мение, Фред Куммеров утверждает, что это не диетический холестерин, а оксистерины или окисленный холестерин из жареной пищи и курения, которые являются виновниками.[52]
Прогорклые жиры и масла очень неприятны на вкус даже в небольших количествах, поэтому люди избегают их есть.[53]Очень сложно измерить или оценить фактическое потребление этих веществ человеком.[54] Высоконенасыщенные масла с высоким содержанием омега-3, такие как рыбий жир, при продаже в форме таблеток могут скрыть вкус окисленного или прогорклого жира, который может присутствовать. В США диетические добавки в индустрии здорового питания регулируются самостоятельно и не подпадают под действие правил FDA.[55] Чтобы должным образом защитить ненасыщенные жиры от окисления, лучше всего хранить их в прохладном месте в бескислородной среде.
Патофизиология
Атерогенез - это процесс развития атероматозных бляшек. Он характеризуется ремоделированием артерий, приводящим к субэндотелиальному накоплению жировых веществ, называемых бляшками. Наращивание атероматозной бляшки - это медленный процесс, развивающийся в течение нескольких лет в результате сложной серии клеточных событий, происходящих внутри артериальной стенки и в ответ на множество местных факторов сосудистой циркуляции. Одна недавняя гипотеза предполагает, что по неизвестным причинам лейкоциты, Такие как моноциты или же базофилы, начать атаковать эндотелий просвета артерии в сердечная мышца. Последующий воспаление приводит к образованию атероматозных бляшек в артериальной внутренняя оболочка, участок стенки сосуда, расположенный между эндотелий и туника СМИ. Большая часть этих повреждений состоит из лишнего жира, коллаген, и эластин. Сначала по мере роста бляшек только утолщение стен происходит без сужения. Стеноз является поздним событием, которое может никогда не произойти и часто является результатом повторяющегося разрыва бляшки и реакций заживления, а не только самого атеросклеротического процесса.
Сотовый
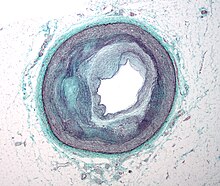
Ранний атерогенез характеризуется прилипанием циркулирующей крови моноциты (тип лейкоцит ) к выстилке сосудистого русла эндотелий, затем путем их миграции в субэндотелиальное пространство и дальнейшей активации в моноцитарные макрофаги.[56] Основным документированным драйвером этого процесса являются частицы окисленных липопротеинов внутри стенки под слоем эндотелиальный клеток, хотя верхняя норма или повышенная концентрация глюкозы в крови также играет важную роль, и не все факторы полностью изучены. Жирные полосы может появляться и исчезать.
Липопротеин низкой плотности (LDL) частицы в плазме крови проникают в эндотелий окисляются, создавая риск сердечно-сосудистые заболевания. Сложный набор биохимических реакций регулирует окисление ЛПНП с участием ферментов (таких как Lp-LpA2 ) и свободные радикалы в эндотелии.
Первоначальное повреждение эндотелия приводит к воспалительной реакции. Моноциты попадают в стенку артерии из кровотока, при этом тромбоциты придерживаясь области оскорбления. Этому может способствовать редокс-сигнализация индукция таких факторов, как VCAM-1, которые привлекают циркулирующие моноциты, и M-CSF, который избирательно необходим для дифференциации моноцитов в макрофаги. Моноциты дифференцируются в макрофаги, которые распространяются локально,[57] проглатывать окисленные ЛПНП, медленно превращаясь в большие "пенные ячейки «- так называемые из-за их измененного внешнего вида в результате многочисленных внутренних цитоплазматических пузырьки и в результате липид содержание. Под микроскопом очаг поражения выглядит как жирная полоса. Пенистые клетки со временем погибают и продолжают воспалительный процесс.
В дополнение к этой клеточной активности также наблюдается пролиферация гладких мышц и миграция из туника СМИ в интима в ответ на цитокины секретируются поврежденными эндотелиальными клетками. Это вызывает образование фиброзной капсулы, покрывающей жировую полоску. Неповрежденный эндотелий может предотвратить разрастание гладких мышц, высвобождая оксид азота.
Кальцификация и липиды
Кальцификация формы среди гладкие мышцы сосудов клетки окружающего мышечного слоя, особенно в мышечных клетках, прилегающих к атеромам, и на поверхности атеромных бляшек и тканей.[58] Со временем, когда клетки умирают, это приводит к отложению внеклеточного кальция между мышечной стенкой и внешней частью атероматозных бляшек. Поскольку атероматозная бляшка препятствует регулированию отложения кальция, она накапливается и кристаллизуется. Подобная форма интрамуральной кальцификации, представляющая картину ранней фазы артериосклероза, по-видимому, вызывается рядом лекарств, которые обладают антипролиферативным механизмом действия (Райнер Лидтке 2008).
Холестерин доставляется в стенку сосуда холестеринсодержащим липопротеин низкой плотности (ЛПНП) частицы. Чтобы привлечь и стимулировать макрофаги, холестерин должен высвобождаться из частиц ЛПНП и окисляться, что является ключевым этапом продолжающегося воспалительного процесса. Процесс усугубляется, если недостаточно липопротеин высокой плотности (ЛПВП), липопротеиновая частица, которая удаляет холестерин из тканей и переносит его обратно в печень.
Пенистые клетки и тромбоциты способствуют миграции и распространению гладкая мышца клетки, которые, в свою очередь, поглощают липиды, заменяются коллагеном и сами превращаются в пенистые клетки. Защитный фиброзный колпачок обычно образуется между жировыми отложениями и выстилкой артерии ( интима ).
Эти закрытые жировые отложения (теперь называемые атеромами) вырабатывают ферменты, которые со временем вызывают расширение артерии. Пока артерия увеличивается достаточно, чтобы компенсировать лишнюю толщину атеромы, сужения нет ("стеноз ") отверстия (" просвет "). Артерия расширяется и приобретает яйцевидное поперечное сечение, но с круглым отверстием. Если увеличение не пропорционально толщине атеромы, то аневризма создано.[59]
Видимые особенности
Хотя артерии обычно не исследуются под микроскопом, можно выделить два типа бляшек:[60]
- Фибролипидная (фиброзно-жировая) бляшка характеризуется накоплением липидных клеток под интимой артерии, обычно без сужения просвета из-за компенсаторного расширения ограничивающего мышечного слоя стенки артерии. Под эндотелием находится «фиброзный колпачок», покрывающий атероматозное «ядро» бляшки. Ядро состоит из нагруженных липидами клеток (макрофагов и гладкомышечных клеток) с повышенным содержанием холестерина в тканях и сложного эфира холестерина, фибрина, протеогликанов, коллагена, эластина и клеточного мусора. В запущенных бляшках центральное ядро бляшки обычно содержит внеклеточные отложения холестерина (высвобождаемые из мертвых клеток), которые образуют области кристаллов холестерина с пустыми игольчатыми щелями. По периферии бляшки находятся более молодые «пенистые» клетки и капилляры. Эти бляшки обычно наносят наибольший урон человеку при разрыве. Кристаллы холестерина также могут играть роль.[61]
- Фиброзный налет также локализуется под интимой, внутри стенки артерии, что приводит к утолщению и расширению стенки, а иногда и к пятнистому локализованному сужению просвета с некоторой атрофией мышечного слоя. Фиброзный налет содержит коллагеновые волокна (эозинофильные), осадки кальция (гематоксилинофильные) и, реже, клетки, содержащие липиды.
Фактически, мышечная часть стенки артерии образует небольшой аневризмы достаточно большой, чтобы вместить атерома которые присутствуют. Мышечные части стенок артерий обычно остаются сильными даже после того, как они реконструируются, чтобы компенсировать атероматозные бляшки.
Однако атеромы в стенке сосуда мягкие и хрупкие, с небольшой эластичностью. Артерии постоянно расширяются и сужаются с каждым ударом сердца, т. Е. С пульсом. Кроме того, отложения кальцинации между внешней частью атеромы и мышечной стенкой по мере их развития приводят к потере эластичности и жесткости артерии в целом.
Отложения кальцификации,[62] после того, как они стали достаточно развитыми, частично видны на коронарной артерии компьютерная томография или же электронно-лучевая томография (EBT) в виде колец с повышенной рентгенографической плотностью, образующих ореолы вокруг внешних краев атероматозных бляшек внутри стенки артерии. На CT> 130 единиц на Шкала Хаунсфилда (некоторые утверждают, что 90 единиц) - это рентгенографическая плотность, обычно принимаемая как отчетливо представляющая кальцификацию тканей внутри артерий. Эти отложения демонстрируют недвусмысленное свидетельство заболевания, относительно запущенного, даже несмотря на то, что просвет артерии часто остается нормальным по данным ангиографии.
Разрыв и стеноз

Хотя заболевание имеет тенденцию медленно прогрессировать в течение десятилетий, обычно оно остается бессимптомным до появления атеромы. изъязвления, что приводит к немедленному свертыванию крови на месте язвы атеромы. Это запускает каскад событий, который приводит к увеличению сгустка, который может быстро препятствовать току крови. Полная блокада приводит к ишемии миокардиальной (сердечной) мышцы и повреждению. Этот процесс - инфаркт миокарда или «сердечный приступ».
Если сердечный приступ не является смертельным, возникает фиброзная организация сгустка внутри просвета, закрывающая разрыв, но также вызывающая стеноз или закрытие просвета, или с течением времени и после повторных разрывов, что приводит к стойкому, обычно локализованному стенозу или закупорке просвета артерии. Стенозы могут прогрессировать медленно, тогда как изъязвление бляшек - это внезапное явление, которое возникает особенно при атеромах с более тонкими / более слабыми фиброзными крышками, которые стали «нестабильными».
Повторяющиеся разрывы бляшек, не приводящие к полному закрытию просвета, в сочетании с наложением сгустка на разрыв и реакцией заживления для стабилизации сгустка - это процесс, который с течением времени вызывает большинство стенозов. Стенотические области имеют тенденцию становиться более стабильными, несмотря на увеличение скорости потока в этих сужениях. Большинство серьезных событий, связанных с остановкой кровотока, происходит на больших бляшках, которые до их разрыва вызывали очень незначительный стеноз или вообще не вызывали его.
По данным клинических испытаний, 20% - это средний стеноз бляшек, которые впоследствии разрываются, что приводит к полному закрытию артерии. Наиболее серьезные клинические проявления не возникают на бляшках, вызывающих стеноз высокой степени. По данным клинических испытаний, только 14% сердечных приступов происходят из-за закрытия артерии бляшками, вызывающими стеноз 75% или более до закрытия сосуда.[нужна цитата ]
Если фиброзный колпачок, отделяющий мягкую атерому от кровотока внутри артерии, разрывается, фрагменты ткани обнажаются и высвобождаются. Эти фрагменты ткани сильно способствуют образованию тромбов и содержат коллаген и тканевый фактор; они активируют тромбоциты и активируйте система коагуляции. В результате образуется тромб (сгусток крови), лежащий над атеромой, который сильно затрудняет кровоток. Из-за препятствия кровотоку нижележащие ткани лишаются кислород и питательные вещества. Если это миокард (сердечная мышца) стенокардия (сердечная боль в груди) или инфаркт миокарда (сердечный приступ) развивается.
Ускоренный рост бляшек
Распределение атеросклеротических бляшек в части артериального эндотелия неоднородно. Множественное и очаговое развитие атеросклеротических изменений аналогично развитию амилоидных бляшек в головном мозге и возрастных пятен на коже. Теория старения из-за неправильного ремонта предполагает, что механизмы неправильного ремонта[63][64] играют важную роль в очаговом развитии атеросклероза.[65] Образование бляшки - результат восстановления поврежденного эндотелия. Из-за вливания липидов в субэндотелий восстановление должно закончиться измененным ремоделированием местного эндотелия. Это проявление некачественного ремонта. Важно то, что это измененное ремоделирование делает местный эндотелий более хрупким к повреждениям и снижает эффективность восстановления. Как следствие, эта часть эндотелия имеет повышенный риск травмирования и неправильного ремонта. Таким образом, накопление неправильных ремонтов эндотелия является локализованным и самоускоряющимся. Таким образом, рост налета также ускоряется. В пределах части артериальной стенки самая старая бляшка всегда самая большая и самая опасная из-за закупорки местной артерии.
Составные части
Зубной налет делится на три отдельных компонента:
- В атерома («кусок кашицы», от Греческий ἀθήρα (атера) 'каша '), который представляет собой узелковое скопление мягкого хлопьевидного желтоватого материала в центре больших бляшек, состоящих из макрофагов, ближайших к просвет артерии
- Подлежащие области кристаллов холестерина
- Кальциноз на внешней основе у пожилых или более продвинутых поражения. Атеросклеротические поражения или атеросклеротические бляшки делятся на две широкие категории: стабильные и нестабильные (также называемые уязвимыми).[66] Патобиология атеросклеротических поражений очень сложна, но обычно стабильные атеросклеротические бляшки, которые, как правило, протекают бессимптомно, богаты внеклеточный матрикс и гладкомышечные клетки. С другой стороны, нестабильные бляшки богаты макрофагами и пенные ячейки, и внеклеточный матрикс, отделяющий поражение от просвета артерии (также известный как фиброзный колпачок ) обычно слабая и склонна к разрыву.[67] Разрывы фиброзной капсулы обнажают тромбогенный материал, такой как коллаген,[68] в кровообращение и в конечном итоге вызвать тромб образование в просвете. После образования внутрипросветные тромбы могут полностью закупорить артерии (например, коронарная окклюзия), но чаще они отслаиваются, переходят в кровоток и, в конечном итоге, закупоривают более мелкие нижележащие ветви, вызывая тромбоэмболия.
Помимо тромбоэмболии, хронически расширяющиеся атеросклеротические поражения могут вызвать полное закрытие просвета. Хронически расширяющиеся очаги часто протекают бессимптомно до просвета. стеноз настолько серьезен (обычно более 80%), что кровоснабжение нижележащих тканей оказывается недостаточным, что приводит к ишемия. Эти осложнения прогрессирующего атеросклероза являются хроническими, медленно прогрессирующими и кумулятивными. Чаще всего мягкий налет разрывается внезапно (см. уязвимая бляшка ), вызывая образование тромба, который будет быстро замедлять или останавливать кровоток, что приводит к гибели тканей, питаемых артерией, примерно за пять минут. Это событие называется инфаркт.
Диагностика


Участки сильного сужения, стеноз, обнаруживается ангиография, и в меньшей степени "Стресс-тестирование "долгое время находились в центре внимания методов диагностики человека для сердечно-сосудистые заболевания, в целом. Однако эти методы ориентированы на обнаружение только серьезного сужения, а не основного заболевания атеросклерозом. Как показали клинические исследования на людях, наиболее тяжелые события происходят в местах с тяжелым налетом, но при этом незначительное сужение просвета или его отсутствие до того, как внезапно возникнут изнуряющие события. Разрыв бляшки может привести к закупорке просвета артерии в течение нескольких секунд или минут, а также к потенциальной необратимой слабости, а иногда и к внезапной смерти.
Разорвавшиеся бляшки называются сложными бляшками. В внеклеточный матрикс поражения разрывается, обычно на плече фиброзной капсулы, отделяющей поражение от просвета артерии, где обнажаются тромбогенные компоненты бляшки, в основном коллаген вызовет тромб формирование. Затем тромб перемещается вниз по течению к другим кровеносным сосудам, где сгусток крови может частично или полностью блокировать кровоток. Если кровоток полностью заблокирован, происходит гибель клеток из-за отсутствия кислород снабжение соседними ячейками, в результате чего некроз. Сужение или затруднение кровотока может произойти в любой артерии тела. Обструкция артерий, снабжающих сердечную мышцу, приводит к острое сердечно-сосудистое заболевание, в то время как закупорка артерий, снабжающих мозг, приводит к ишемической Инсульт.

Стеноз просвета более 75% в прошлом считался признаком клинически значимого заболевания из-за повторяющихся эпизодов стенокардия и аномалии в стресс-тесты обнаруживаются только при такой степени тяжести стеноза. Однако клинические испытания показали, что только около 14% клинически изнурительных событий происходит на участках со стенозом более 75%. Большинство сердечно-сосудистых событий, связанных с внезапным разрывом атеромной бляшки, не демонстрируют явного сужения просвета. Таким образом, с конца 1990-х годов большее внимание уделяется «уязвимой бляшке».[69]
Помимо традиционных диагностических методов, таких как ангиография и стресс-тестирование, в последние десятилетия были разработаны другие методы обнаружения для более раннего выявления атеросклеротического заболевания. Некоторые из подходов к обнаружению включают анатомическое обнаружение и физиологическое измерение.
Примеры анатомических методов обнаружения включают оценку кальция в коронарных артериях с помощью КТ, ТИМ сонных артерий (толщина интимы медиа ) измерение ультразвуком, и внутрисосудистое ультразвуковое исследование (ВСУЗИ). Примеры физиологических методов измерения включают анализ подкласса липопротеинов, HbA1c, hs-CRP, и гомоцистеин Как анатомические, так и физиологические методы позволяют раннее обнаружение до появления симптомов, определение стадии заболевания и отслеживание его прогрессирования. Анатомические методы более дорогие, и некоторые из них носят инвазивный характер, например, ВСУЗИ. С другой стороны, физиологические методы зачастую дешевле и безопаснее. Но они не позволяют количественно оценить текущее состояние болезни и напрямую не отслеживать прогрессирование. В последние годы развитие методов ядерной визуализации, таких как ПЭТ и ОФЭКТ, предоставило способы оценки степени тяжести атеросклеротических бляшек.
Профилактика
До 90% сердечно-сосудистых заболеваний можно предотвратить, если избегать установленных факторов риска.[70][71] Медицинское лечение атеросклероза в первую очередь включает изменение факторов риска, например, отказ от курения и ограничение диеты. В этом случае профилактика обычно заключается в правильном питании, физических упражнениях, отказе от курения и поддержании нормального веса.[4]
Рацион питания
Изменения в диете могут помочь предотвратить развитие атеросклероза. Предварительные данные свидетельствуют о том, что диета, содержащая молочные продукты, не влияет или не снижает риск сердечно-сосудистые заболевания.[72][73]
Диета с высоким содержанием фруктов и овощей снижает риск сердечно-сосудистых заболеваний и смерти.[74] Данные свидетельствуют о том, что средиземноморская диета может улучшить сердечно-сосудистые результаты.[75] Есть также свидетельства того, что средиземноморская диета может быть лучше, чем нежирная диета в достижении долгосрочных изменений факторов риска сердечно-сосудистых заболеваний (например, снижение уровень холестерина и артериальное давление ).[76]
Упражнение
Контролируемая программа упражнений борется с атеросклерозом за счет улучшения кровообращения и функциональности сосудов. Упражнения также используются для контроля веса у пациентов с ожирением, снижения артериального давления и холестерина. Часто изменение образа жизни сочетается с медикаментозной терапией. Например, статины помогают снизить уровень холестерина, антиагреганты, такие как аспирин помогают предотвратить образование тромбов, а для контроля артериального давления обычно используются различные гипотензивные препараты. Если совместных усилий по модификации факторов риска и медикаментозной терапии недостаточно для контроля симптомов или борьбы с неминуемой угрозой ишемических событий, врач может прибегнуть к интервенционным или хирургическим процедурам для устранения обструкции.[77]
Уход
Лечение установленного заболевания может включать лекарства для снижения уровня холестерина, такие как статины, лекарства от кровяного давления или лекарства, снижающие свертываемость, например аспирин.[5] Также может быть проведен ряд процедур, таких как чрезкожное коронарное вмешательство, шунтирование коронарной артерии, или же каротидная эндартерэктомия.[5]
Медицинское лечение часто направлено на облегчение симптомов. Однако меры, направленные на уменьшение основного атеросклероза - в отличие от простого лечения симптомов - более эффективны.[78] Немедикаментозные средства обычно являются первым методом лечения, например, отказ от курения и регулярные физические упражнения.[79][80] Если эти методы не работают, лекарства обычно являются следующим шагом в лечении сердечно-сосудистых заболеваний и, с улучшением, все чаще становятся наиболее эффективным методом в долгосрочной перспективе.
Ключом к более эффективным подходам является сочетание нескольких различных стратегий лечения.[81] Кроме того, для таких подходов, как поведение транспорта липопротеинов, которое, как было показано, дает наибольший успех, принятие более агрессивных стратегий комбинированного лечения, принимаемых на ежедневной основе и на неопределенный срок, обычно дает лучшие результаты, как до, так и особенно после того, как у людей появились симптомы .[78]
Статины
Группа препаратов, именуемая статины широко назначаются для лечения атеросклероза. Они показали преимущество в снижении сердечно-сосудистых заболеваний и смертности у людей с высокое содержание холестерина с небольшими побочными эффектами.[82]
Эти данные в основном относятся к мужчинам среднего возраста, и выводы менее однозначны для женщин и людей старше 70 лет.[83]
Хирургия
Когда атеросклероз стал серьезным и вызвал необратимые ишемия, Такие как потеря ткани в случае заболевание периферических артерий, может быть показано хирургическое вмешательство. Сосудистое шунтирование может восстановить кровоток вокруг пораженного сегмента артерии и ангиопластика с или без стентирование может повторно открыть суженные артерии и улучшить кровоток. Аортокоронарное шунтирование без манипуляции с восходящей аортой продемонстрировало снижение частоты послеоперационного инсульта и смертности по сравнению с традиционной коронарной реваскуляризацией с помпой.[84]
Другой
Имеются данные о том, что некоторые антикоагулянты, особенно варфарин, которые ингибируют образование сгустков, вмешиваясь в метаболизм витамина К, могут действительно способствовать кальцификации артерий в долгосрочной перспективе, несмотря на сокращение образования сгустков в краткосрочной перспективе. Кроме того, отдельные пептиды, такие как 3-гидроксибензальдегид и протокатеховый альдегид, показали васкулопротекторные эффекты, снижающие риск атеросклероза.[85][86][87][88][89]
Эпидемиология
Сердечно-сосудистые заболевания, которые преимущественно являются клиническим проявлением атеросклероза, являются ведущей причиной смерти во всем мире.[90]
Экономика
В 2011 году коронарный атеросклероз входил в десятку самых дорогих состояний, наблюдаемых во время стационарных госпитализаций в США, с совокупными расходами на стационарное лечение в размере 10,4 миллиарда долларов.[91]
Исследование
Липиды
Указание на роль липопротеин высокой плотности (HDL) на атеросклероз был связан с редким человеческим генетическим вариантом Apo-A1 Milano этого белка HDL. Небольшое краткосрочное испытание с использованием синтезированного бактериями человека Apo-A1 Milano ЛПВП у людей с нестабильной стенокардией вызывали довольно резкое снижение измеренного объема коронарных бляшек всего за шесть недель по сравнению с обычным увеличением объема бляшек у пациентов, рандомизированных для плацебо. Испытание было опубликовано в JAMA в начале 2006 г.[нужна цитата ] Текущая работа, начатая в 1990-х годах, может привести к клиническим испытаниям на людях - вероятно, примерно к 2008 году.[нуждается в обновлении ] Они могут использовать синтезированный Apo-A1 Milano HDL напрямую или они могут использовать методы переноса генов для передачи способности синтезировать Apo-A1 Milano HDLipoprotein.[нужна цитата ]
В настоящее время разрабатываются и исследуются методы увеличения концентрации частиц ЛПВП, которые в некоторых исследованиях на животных в значительной степени обращают вспять и удаляют атеромы.[нужна цитата ] Однако повышение ЛПВП любыми способами не обязательно помогает. Например, препарат торцетрапиб это самый эффективный агент, известный в настоящее время для повышения уровня ЛПВП (до 60%). Однако в клинических испытаниях он также увеличил смертность на 60%. Все исследования этого препарата были прекращены в декабре 2006 года.[92] Видеть Ингибитор CETP для подобных подходов.
Действие макрофагов стимулирует прогрессирование атеросклеротической бляшки.Иммуномодуляция атеросклероза это термин для методов, которые модулируют функцию иммунной системы для подавления этого действия макрофагов.[93]
Исследования генетической экспрессии и механизмов контроля продолжаются. Темы включают:
- PPAR, который, как известно, важен для сахара в крови и вариантов производства и функции липопротеинов;[нужна цитата ]
- Множественные варианты белков, которые образуют частицы транспорта липопротеинов.[нужна цитата ]
Участие перекисное окисление липидов цепная реакция в атерогенезе[94] положило начало исследованиям защитной роли тяжелого изотопа (дейтерированный ) полиненасыщенные жирные кислоты (D-PUFA), которые менее склонны к окислению, чем обычные PUFA (H-PUFA). ПНЖК являются основные питательные вещества - они участвуют в метаболизме именно в той форме, в которой потребляются с пищей. В трансгенные мыши, которые являются моделью метаболизма липопротеинов, подобных человеку, добавление D-ПНЖК в рацион действительно снижает прибавку в весе, улучшает обработку холестерина и снижает атеросклеротическое повреждение аорты.[95][96]
miRNA
МикроРНК (миРНК) имеют комплементарные последовательности в 3 'UTR и 5 'UTR of target mRNAs of protein-coding genes, and cause mRNA cleavage or repression of translational machinery. In diseased vascular vessels, miRNAs are dysregulated and highly expressed. miR-33 is found in cardiovascular diseases.[97] It is involved in atherosclerotic initiation and progression including lipid metabolism, insulin signaling and glucose homeostatis, cell type progression and proliferation, and myeloid cell differentiation. It was found in rodents that the inhibition of miR-33 will raise HDL level and the expression of miR-33 is down-regulated in humans with atherosclerotic plaques.[98][99][100]
miR-33a and miR-33b are located on intron 16 of human sterol regulatory element-binding protein 2 (SREBP2) gene on chromosome 22 and intron 17 of SREBP1 gene on chromosome 17.[101] miR-33a/b regulates cholesterol/lipid homeostatis by binding in the 3’UTRs of genes involved in cholesterol transport such as ATP binding cassette (ABC) transporters and enhance or represses its expression. Study have shown that ABCA1 mediates transport of cholesterol from peripheral tissues to Apolipoprotein-1 and it is also important in the reverse cholesterol transport pathway, where cholesterol is delivered from peripheral tissue to the liver, where it can be excreted into bile or converted to bile acids prior to excretion.[97] Therefore, we know that ABCA1 plays an important role in preventing cholesterol accumulation in macrophages. By enhancing miR-33 function, the level of ABCA1 is decreased, leading to decrease cellular cholesterol efflux to apoA-1. On the other hand, by inhibiting miR-33 function, the level of ABCA1 is increased and increases the cholesterol efflux to apoA-1. Suppression of miR-33 will lead to less cellular cholesterol and higher plasma HDL level through the regulation of ABCA1 expression.[102]
The sugar, циклодекстрин, removed cholesterol that had built up in the arteries of mice fed a high-fat diet.[103]
Повреждение ДНК
Старение is the most important risk factor for cardiovascular problems. The causative basis by which aging mediates its impact, independently of other recognized risk factors, remains to be determined. Evidence has been reviewed for a key role of Повреждение ДНК in vascular aging.[104][105][106] 8-oxoG, a common type of oxidative damage in ДНК, is found to accumulate in plaque vascular smooth muscle клетки макрофаги и endothelial cells,[107] thus linking DNA damage to plaque formation. DNA strand breaks also increased in atherosclerotic plaques.[107] Werner syndrome (WS) is a premature aging condition in humans.[108] WS is caused by a genetic defect in a RecQ геликаза that is employed in several repair processes that remove damages from DNA. WS patients develop a considerable burden of atherosclerotic plaques in their coronary arteries и аорта: calcification of the aortic valve is also frequently observed.[105] These findings link excessive unrepaired DNA damage to premature aging and early atherosclerotic plaque development (see Теория повреждений ДНК старения ).
Микроорганизмы
В микробиота - все микроорганизмы in the body, can contribute to atherosclerosis in many ways: modulation of the иммунная система, изменения в метаболизм, processing of nutrients and production of certain metabolites that can get into blood circulation.[109] One such metabolite, produced by кишечные бактерии, является trimethylamine N-oxide (ТМАО). Its levels have been associated with atherosclerosis in human studies and animal research suggest that there can be a causal relation. An association between the bacterial genes encoding trimethylamine lyases — the ферменты involved in TMAO generation — and atherosclerosis has been noted.[110][109]
Клетки гладких мышц сосудов
Клетки гладких мышц сосудов play a key role in atherogenesis and were historically considered to be beneficial for plaque stability by forming a protective fibrous cap and synthesising strength-giving внеклеточный матрикс составные части.[111][112] However, in addition to the fibrous cap, vascular smooth muscle cells also give rise to many of the cell types found within the plaque core and can modulate their phenotype to both promote and reduce plaque stability.[111][113][114][115] Vascular smooth muscle cells exhibit pronounced plasticity within atherosclerotic plaque and can modify their gene expression profile to resemble various other cell types, including макрофаги, myofibroblasts, mesenchymal stem cells and osteochondrocytes.[116][117][111] Importantly, genetic lineage‐tracing experiments have unequivocally shown that 40-90% of plaque-resident cells are vascular smooth muscle cell derived.[118][115] Therefore, it is important to research the role of vascular smooth muscle cells in atherosclerosis to identify new therapeutic targets.
Рекомендации
- ^ а б c d е ж "What Are the Signs and Symptoms of Atherosclerosis? - NHLBI, NIH". www.nhlbi.nih.gov. 22 июня 2016 г.. Получено 5 ноября 2017.
- ^ а б "What Causes Atherosclerosis? - NHLBI, NIH". www.nhlbi.nih.gov. 22 июня 2016 г.. Получено 6 ноября 2017.
- ^ а б c "Who Is at Risk for Atherosclerosis?". www.nhlbi.nih.gov. 22 июня 2016 г.. Получено 5 ноября 2017.
- ^ а б c "How Can Atherosclerosis Be Prevented or Delayed? - NHLBI, NIH". www.nhlbi.nih.gov. 22 июня 2016 г.. Получено 6 ноября 2017.
- ^ а б c d е "How Is Atherosclerosis Treated? - NHLBI, NIH". www.nhlbi.nih.gov. 22 июня 2016 г.. Получено 6 ноября 2017.
- ^ а б Aronow WS, Fleg JL, Rich MW (2013). Tresch and Aronow's Cardiovascular Disease in the Elderly, Fifth Edition. CRC Press. п. 171. ISBN 9781842145449.
- ^ а б c "What Is Atherosclerosis? - NHLBI, NIH". www.nhlbi.nih.gov. 22 июня 2016 г.. Получено 6 ноября 2017.
- ^ Lind, L (August 2003). "Circulating markers of inflammation and atherosclerosis". Атеросклероз. 169 (2): 203–214. Дои:10.1016/S0021-9150(03)00012-1.
- ^ "How Is Atherosclerosis Diagnosed? - NHLBI, NIH". www.nhlbi.nih.gov. 22 июня 2016 г.. Получено 6 ноября 2017.
- ^ Topol EJ, Califf RM (2007). Учебник сердечно-сосудистой медицины. Липпинкотт Уильямс и Уилкинс. п. 2. ISBN 9780781770125.
- ^ а б Shor A (2008). Chlamydia Atherosclerosis Lesion: Discovery, Diagnosis and Treatment. Springer Science & Business Media. п. 8. ISBN 9781846288104.
- ^ "Atherogenic". Словарь Merriam-Webster.
- ^ Ross R (April 1993). "The pathogenesis of atherosclerosis: a perspective for the 1990s". Природа. 362 (6423): 801–9. Bibcode:1993Natur.362..801R. Дои:10.1038/362801a0. PMID 8479518. S2CID 4282916.
- ^ Atherosclerosis. Harvard Health Publications Harvard Health Publications. Health Topics A – Z, (2011)
- ^ а б c "Атеросклероз". National Heart, Lung and Blood Institute. 2011 г.
- ^ а б Velican, Doina; Velican, C. (June 1979). "Study of fibrous plaques occurring in the coronary arteries of children". Атеросклероз. 33 (2): 201–215. Дои:10.1016/0021-9150(79)90117-5. ISSN 0021-9150.
- ^ Stary, H C; Chandler, A B; Glagov, S; Guyton, J R; Insull, W; Rosenfeld, M E; Schaffer, S A; Schwartz, C J; Wagner, W D; Wissler, R W (May 1994). "A definition of initial, fatty streak, and intermediate lesions of atherosclerosis. A report from the Committee on Vascular Lesions of the Council on Arteriosclerosis, American Heart Association". Тираж. 89 (5): 2462–2478. Дои:10.1161/01.CIR.89.5.2462. ISSN 0009-7322.
- ^ "First signs of atherosclerotic heart disease may appear in early childhood". Новости-Medical.net.
- ^ Flora GC, Baker AB, Loewenson RB, Klassen AC (November 1968). "A comparative study of cerebral atherosclerosis in males and females". Тираж. 38 (5): 859–69. Дои:10.1161/01.CIR.38.5.859. PMID 5697685.
- ^ а б Arrhythmia. Heart and Stroke Foundation. «Архивная копия». Архивировано из оригинал на 2014-02-03. Получено 2014-01-31.CS1 maint: заархивированная копия как заголовок (связь) (2011)
- ^ Sims NR, Muyderman H (January 2010). "Mitochondria, oxidative metabolism and cell death in stroke" (PDF). Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease. 1802 (1): 80–91. Дои:10.1016/j.bbadis.2009.09.003. PMID 19751827.
- ^ Enos WF, Holmes RH, Beyer J (1953). "Coronary disease among United States soldiers killed in action in Korea: Preliminary Report". JAMA. 152 (12): 1090–93. Дои:10.1001/jama.1953.03690120006002. PMID 13052433. The average age was calculated from the ages of 200 of the soldiers. No age was recorded in nearly 100 of the men.
- ^ Li X, Fang P, Li Y, Kuo YM, Andrews AJ, Nanayakkara G, Johnson C, Fu H, Shan H, Du F, Hoffman NE, Yu D, Eguchi S, Madesh M, Koch WJ, Sun J, Jiang X, Wang H, Yang X (June 2016). "Mitochondrial Reactive Oxygen Species Mediate Lysophosphatidylcholine-Induced Endothelial Cell Activation". Артериосклероз, тромбоз и биология сосудов. 36 (6): 1090–100. Дои:10.1161/ATVBAHA.115.306964. ЧВК 4882253. PMID 27127201.
- ^ Williams KJ, Tabas I (May 1995). "The response-to-retention hypothesis of early atherogenesis". Артериосклероз, тромбоз и биология сосудов. 15 (5): 551–61. Дои:10.1161/01.ATV.15.5.551. ЧВК 2924812. PMID 7749869.
- ^ Aviram M, Fuhrman B (November 1998). "LDL oxidation by arterial wall macrophages depends on the oxidative status in the lipoprotein and in the cells: role of prooxidants vs. antioxidants". Молекулярная и клеточная биохимия. 188 (1–2): 149–59. Дои:10.1023/A:1006841011201. PMID 9823020. S2CID 12222110.
- ^ Campbell LA, Rosenfeld ME (July 2015). "Infection and Atherosclerosis Development". Arch Med Res. 46 (5): 339–50. Дои:10.1016/j.arcmed.2015.05.006. ЧВК 4524506. PMID 26004263.
- ^ а б c d е ж грамм час я j k л м п о п q р https://www.nhlbi.nih.gov/health/health-topics/topics/atherosclerosis/atrisk
- ^ Sinha A, Feinstein MJ (March 2019). "Coronary Artery Disease Manifestations in HIV: What, How, and Why". The Canadian Journal of Cardiology. 35 (3): 270–279. Дои:10.1016/j.cjca.2018.11.029. PMID 30825949.
- ^ Tyrrell DJ, Blin MB, Song J, Wood SC, Zhang M, Beard DA, Goldstein DR (January 2020). "Age-Associated Mitochondrial Dysfunction Accelerates Atherogenesis". Циркуляционные исследования. 126 (3): 298–314. Дои:10.1161/CIRCRESAHA.119.315644. ЧВК 7006722. PMID 31818196.
- ^ VELICAN, C; VELICAN, D (March 1985). "Differences in the pattern of atherosclerotic involvement between non-branched regions and adjacent branching points of human coronary arteries". Атеросклероз. 54 (3): 333–342. Дои:10.1016/0021-9150(85)90126-1. ISSN 0021-9150.
- ^ Enas EA, Kuruvila A, Khanna P, Pitchumoni CS, Mohan V (October 2013). "Benefits & risks of statin therapy for primary prevention of cardiovascular disease in Asian Indians - a population with the highest risk of premature coronary artery disease & diabetes". Индийский журнал медицинских исследований. 138 (4): 461–91. ЧВК 3868060. PMID 24434254.
- ^ Indian Heart Association Why South Asians Facts Web. 30 апреля 2015 г. http://indianheartassociation.org/why-indians-why-south-asians/overview/
- ^ Borissoff JI, Spronk HM, Heeneman S, ten Cate H (June 2009). "Is thrombin a key player in the 'coagulation-atherogenesis' maze?". Сердечно-сосудистые исследования. 82 (3): 392–403. Дои:10.1093/cvr/cvp066. PMID 19228706.
- ^ Borissoff JI, Heeneman S, Kilinç E, Kassák P, Van Oerle R, Winckers K, Govers-Riemslag JW, Hamulyák K, Hackeng TM, Daemen MJ, ten Cate H, Spronk HM (August 2010). "Early atherosclerosis exhibits an enhanced procoagulant state". Тираж. 122 (8): 821–30. Дои:10.1161/CIRCULATIONAHA.109.907121. PMID 20697022.
- ^ Borissoff JI, Spronk HM, ten Cate H (May 2011). "The hemostatic system as a modulator of atherosclerosis". Медицинский журнал Новой Англии. 364 (18): 1746–60. Дои:10.1056/NEJMra1011670. PMID 21542745.
- ^ Food and nutrition board, institute of medicine of the national academies (2005). Нормы потребления энергии, углеводов, клетчатки, жиров, жирных кислот, холестерина, белков и аминокислот (макроэлементов) с пищей. Национальная академия прессы. С. 481–484.
- ^ Mozaffarian D, Rimm EB, Herrington DM (November 2004). "Dietary fats, carbohydrate, and progression of coronary atherosclerosis in postmenopausal women". Американский журнал клинического питания. 80 (5): 1175–84. Дои:10.1093/ajcn/80.5.1175. ЧВК 1270002. PMID 15531663.
- ^ Bhatt DL, Topol EJ (July 2002). "Need to test the arterial inflammation hypothesis". Тираж. 106 (1): 136–40. Дои:10.1161/01.CIR.0000021112.29409.A2. PMID 12093783.
- ^ Griffin M, Frazer A, Johnson A, Collins P, Owens D, Tomkin GH (June 1998). "Cellular cholesterol synthesis--the relationship to post-prandial glucose and insulin following weight loss". Атеросклероз. 138 (2): 313–8. Дои:10.1016/S0021-9150(98)00036-7. PMID 9690914.
- ^ King CR, Knutson KL, Rathouz PJ, Sidney S, Liu K, Lauderdale DS (December 2008). "Short sleep duration and incident coronary artery calcification". JAMA. 300 (24): 2859–66. Дои:10.1001/jama.2008.867. ЧВК 2661105. PMID 19109114.
- ^ Provost EB, Madhloum N, Int Panis L, De Boever P, Nawrot TS (2015). "Carotid intima-media thickness, a marker of subclinical atherosclerosis, and particulate air pollution exposure: the meta-analytical evidence". PLOS ONE. 10 (5): e0127014. Bibcode:2015PLoSO..1027014P. Дои:10.1371/journal.pone.0127014. ЧВК 4430520. PMID 25970426.
- ^ Adar SD, Sheppard L, Vedal S, Polak JF, Sampson PD, Diez Roux AV, Budoff M, Jacobs DR, Barr RG, Watson K, Kaufman JD (April 23, 2013). "Fine particulate air pollution and the progression of carotid intima-medial thickness: a prospective cohort study from the multi-ethnic study of atherosclerosis and air pollution". PLOS Медицина. 10 (4): e1001430. Дои:10.1371/journal.pmed.1001430. ЧВК 3637008. PMID 23637576.
This early analysis from MESA suggests that higher long-term PM2.5 concentrations are associated with increased IMT progression and that greater reductions in PM2.5 are related to slower IMT progression.
- ^ Chih-Hao Wang. "Biological Gradient Between Long-Term Arsenic Exposure and Carotid Atherosclerosis". ahajournals.org.
- ^ "Treating Hypothyroidism Reduces Atherosclerosis Risk". Американский семейный врач. 69 (3). 1 февраля 2004 г. ISSN 0002-838X.
- ^ Bale BF, Doneen AL, Vigerust DJ (April 2017). «Пародонтальные патогены высокого риска вносят вклад в патогенез атеросклероза». Последипломный медицинский журнал. 93 (1098): 215–220. Дои:10.1136/postgradmedj-2016-134279. ЧВК 5520251. PMID 27899684.
- ^ Taubes G (March 2001). "Nutrition. The soft science of dietary fat". Наука. 291 (5513): 2536–2545. Дои:10.1126/science.291.5513.2536. PMID 11286266. S2CID 54015137.
- ^ "Food Pyramids: Nutrition Source, Harvard School of Public Health". Архивировано из оригинал 26 декабря 2007 г.. Получено 2007-11-25.
- ^ Staprãns I, Rapp JH, Pan XM, Hardman DA, Feingold KR (April 1996). "Oxidized lipids in the diet accelerate the development of fatty streaks in cholesterol-fed rabbits". Артериосклероз, тромбоз и биология сосудов. 16 (4): 533–8. Дои:10.1161/01.atv.16.4.533. PMID 8624775.
- ^ Song JH, Fujimoto K, Miyazawa T (December 2000). "Polyunsaturated (n-3) fatty acids susceptible to peroxidation are increased in plasma and tissue lipids of rats fed docosahexaenoic acid-containing oils". Журнал питания. 130 (12): 3028–33. Дои:10.1093/jn/130.12.3028. PMID 11110863.
- ^ Yap SC, Choo YM, Hew NF, Yap SF, Khor HT, Ong AS, Goh SH (December 1995). "Oxidative susceptibility of low density lipoprotein from rabbits fed atherogenic diets containing coconut, palm, or soybean oils". Липиды. 30 (12): 1145–50. Дои:10.1007/BF02536616. PMID 8614305. S2CID 3960289.
- ^ Greco AV, Mingrone G (1990). "Serum and biliary lipid pattern in rabbits feeding a diet enriched with unsaturated fatty acids". Experimental Pathology. 40 (1): 19–33. Дои:10.1016/S0232-1513(11)80281-1. PMID 2279534.
- ^ "Scientist, 98, challenges orthodoxy on causes of heart disease". medicalxpress.com.
- ^ Mattes RD (December 2005). "Fat taste and lipid metabolism in humans". Физиология и поведение. 86 (5): 691–7. Дои:10.1016/j.physbeh.2005.08.058. PMID 16249011. S2CID 33916150.
The rancid odor of an oxidized fat is readily detectable
- ^ Dobarganes C, Márquez-Ruiz G (March 2003). "Oxidized fats in foods". Текущее мнение о клиническом питании и метаболическом лечении. 6 (2): 157–63. Дои:10.1097/00075197-200303000-00004. PMID 12589185. S2CID 21085461.
- ^ supplements, FDA. "Dietary Supplements".
- ^ Schwartz CJ, Valente AJ, Sprague EA, Kelley JL, Cayatte AJ, Mowery J (December 1992). "Atherosclerosis. Potential targets for stabilization and regression". Тираж. 86 (6 Suppl): III117–23. PMID 1424045.
- ^ Robbins CS, Hilgendorf I, Weber GF, Theurl I, Iwamoto Y, Figueiredo JL, Gorbatov R, Sukhova GK, Gerhardt LM, Smyth D, Zavitz CC, Shikatani EA, Parsons M, van Rooijen N, Lin HY, Husain M, Libby P, Nahrendorf M, Weissleder R, Swirski FK (September 2013). "Local proliferation dominates lesional macrophage accumulation in atherosclerosis". Природа Медицина. 19 (9): 1166–72. Дои:10.1038/nm.3258. ЧВК 3769444. PMID 23933982.
- ^ Miller JD (June 2013). "Cardiovascular calcification: Orbicular origins". Материалы Природы. 12 (6): 476–8. Bibcode:2013NatMa..12..476M. Дои:10.1038/nmat3663. PMID 23695741.
- ^ Glagov S, Weisenberg E, Zarins CK, Stankunavicius R, Kolettis GJ (May 1987). "Compensatory enlargement of human atherosclerotic coronary arteries". Медицинский журнал Новой Англии. 316 (22): 1371–5. Дои:10.1056 / NEJM198705283162204. PMID 3574413.
- ^ "Coronary atherosclerosis — the fibrous plaque with calcification". www.pathologyatlas.ro. Получено 2010-03-25.
- ^ Janoudi A, Shamoun FE, Kalavakunta JK, Abela GS (July 2016). «Кристаллы холестерина вызывают артериальное воспаление и дестабилизацию атеросклеротической бляшки». Европейский журнал сердца. 37 (25): 1959–67. Дои:10.1093 / eurheartj / ehv653. PMID 26705388.
- ^ Maton A, Hopkins RL, McLaughlin CW, Johnson S, Warner MQ, LaHart D, Wright JD (1993). Биология человека и здоровье. Энглвуд Клиффс, Нью-Джерси: Prentice Hall. ISBN 978-0-13-981176-0. OCLC 32308337.
- ^ Wang J, Michelitsch T, Wunderlin A, Mahadeva R (2009). "Aging as a consequence of Misrepair –a novel theory of aging". 0904 (575). arXiv:0904.0575. Bibcode:2009arXiv0904.0575W. Цитировать журнал требует
| журнал =(помощь) - ^ Wang-Michelitsch J, Michelitsch T (2015). "Aging as a process of accumulation of Misrepairs". 1503 (7163). arXiv:1503.07163. Bibcode:2015arXiv150307163W. Цитировать журнал требует
| журнал =(помощь) - ^ Wang-Michelitsch J, Michelitsch T (2015). "Misrepair mechanism in the development of atherosclerotic plaques". 1505 (1289). arXiv:1505.01289. Bibcode:2015arXiv150501289W. Цитировать журнал требует
| журнал =(помощь) - ^ Ross R (January 1999). "Atherosclerosis--an inflammatory disease". Медицинский журнал Новой Англии. 340 (2): 115–26. Дои:10.1056/NEJM199901143400207. PMID 9887164.
- ^ Finn AV, Nakano M, Narula J, Kolodgie FD, Virmani R (July 2010). "Concept of vulnerable/unstable plaque". Артериосклероз, тромбоз и биология сосудов. 30 (7): 1282–92. Дои:10.1161/ATVBAHA.108.179739. PMID 20554950.
- ^ Didangelos A, Simper D, Monaco C, Mayr M (May 2009). "Proteomics of acute coronary syndromes". Current Atherosclerosis Reports. 11 (3): 188–95. Дои:10.1007/s11883-009-0030-x. PMID 19361350. S2CID 41219190.
- ^ Maseri A, Fuster V (April 2003). "Is there a vulnerable plaque?". Тираж. 107 (16): 2068–71. Дои:10.1161/01.CIR.0000070585.48035.D1. PMID 12719286.
- ^ McGill HC, McMahan CA, Gidding SS (March 2008). "Preventing heart disease in the 21st century: implications of the Pathobiological Determinants of Atherosclerosis in Youth (PDAY) study". Тираж. 117 (9): 1216–27. Дои:10.1161/CIRCULATIONAHA.107.717033. PMID 18316498.
- ^ McNeal CJ, Dajani T, Wilson D, Cassidy-Bushrow AE, Dickerson JB, Ory M (January 2010). "Hypercholesterolemia in youth: opportunities and obstacles to prevent premature atherosclerotic cardiovascular disease". Current Atherosclerosis Reports. 12 (1): 20–8. Дои:10.1007/s11883-009-0072-0. PMID 20425267. S2CID 37833889.
- ^ Rice BH (2014). "Dairy and Cardiovascular Disease: A Review of Recent Observational Research". Current Nutrition Reports. 3 (2): 130–138. Дои:10.1007/s13668-014-0076-4. ЧВК 4006120. PMID 24818071.
- ^ Kratz M, Baars T, Guyenet S (February 2013). "The relationship between high-fat dairy consumption and obesity, cardiovascular, and metabolic disease". Европейский журнал питания. 52 (1): 1–24. Дои:10.1007/s00394-012-0418-1. PMID 22810464. S2CID 1360916.
- ^ Wang X, Ouyang Y, Liu J, Zhu M, Zhao G, Bao W, Hu FB (July 2014). "Fruit and vegetable consumption and mortality from all causes, cardiovascular disease, and cancer: systematic review and dose-response meta-analysis of prospective cohort studies". BMJ. 349: g4490. Дои:10.1136/bmj.g4490. ЧВК 4115152. PMID 25073782.
- ^ Walker C, Reamy BV (April 2009). "Diets for cardiovascular disease prevention: what is the evidence?". Американский семейный врач. 79 (7): 571–8. PMID 19378874.
- ^ Nordmann AJ, Suter-Zimmermann K, Bucher HC, Shai I, Tuttle KR, Estruch R, Briel M (September 2011). "Meta-analysis comparing Mediterranean to low-fat diets for modification of cardiovascular risk factors". Американский журнал медицины. 124 (9): 841–51.e2. Дои:10.1016/j.amjmed.2011.04.024. PMID 21854893.
- ^ "Unit 6: Cardiovascular, Circulatory, and Hematologic Function." Suzane C. Smeltzer, Brenda G. Bare, Janice L Hinkle, Kerry K Cheever. Brunner & Suddarth's Textbook of Medical-Surgical Nursing. Philadelphia: Lippincott Williams & Wilkins, 2010. 682-900. Textbook.
- ^ а б Fonarow G (2003). "Aggressive treatment of atherosclerosis: The time is now". Cleve. Clin. J. Med. 70 (5): 431–434. Дои:10.3949/ccjm.70.5.431. PMID 12785316.
- ^ Ambrose JA, Barua RS (May 2004). "The pathophysiology of cigarette smoking and cardiovascular disease: an update". Журнал Американского колледжа кардиологии. 43 (10): 1731–7. Дои:10.1016/j.jacc.2003.12.047. PMID 15145091.
- ^ Pigozzi F, et al. (2011). "Endothelial (dys)function: the target of physical exercise for prevention and treatment of cardiovascular disease". J. Sports Med. Phys. Фитнес. 51 (2): 260–267. PMID 21681161.
- ^ Koh KK, Han SH, Oh PC, Shin EK, Quon MJ (April 2010). "Combination therapy for treatment or prevention of atherosclerosis: focus on the lipid-RAAS interaction". Атеросклероз. 209 (2): 307–13. Дои:10.1016/j.atherosclerosis.2009.09.007. ЧВК 2962413. PMID 19800624.
- ^ Taylor F, Huffman MD, Macedo AF, Moore TH, Burke M, Davey Smith G, Ward K, Ebrahim S (January 2013). "Statins for the primary prevention of cardiovascular disease". Кокрановская база данных систематических обзоров. 1 (1): CD004816. Дои:10.1002/14651858.CD004816.pub5. ЧВК 6481400. PMID 23440795.
- ^ Vos E, Rose CP (November 2005). "Questioning the benefits of statins". CMAJ. 173 (10): 1207, author reply 1210. Дои:10.1503/cmaj.1050120. ЧВК 1277053. PMID 16275976.
- ^ Zhao DF, Edelman JJ, Seco M, Bannon PG, Wilson MK, Byrom MJ, Thourani V, Lamy A, Taggart DP, Puskas JD, Vallely MP (February 2017). "Coronary Artery Bypass Grafting With and Without Manipulation of the Ascending Aorta: A Network Meta-Analysis". Журнал Американского колледжа кардиологии. 69 (8): 924–936. Дои:10.1016/j.jacc.2016.11.071. PMID 28231944.
- ^ Kong BS, Cho YH, Lee EJ (2014). "G protein-coupled estrogen receptor-1 is involved in the protective effect of protocatechuic aldehyde against endothelial dysfunction". PLoS ONE. 9 (11): e113242. Дои:10.1371/journal.pone.0113242. ЧВК 4239058. PMID 25411835.
- ^ Kong BS, Im SJ, Lee YJ, Cho YH, Do YR, Byun JW, Ku CR, Lee EJ (2016). "Vasculoprotective Effects of 3-Hydroxybenzaldehyde against VSMCs Proliferation and ECs Inflammation". PLoS ONE. 11 (3): e0149394. Дои:10.1371/journal.pone.0149394. ЧВК 4803227. PMID 27002821.
- ^ Price PA, Faus SA, Williamson MK (February 2000). "Warfarin-induced artery calcification is accelerated by growth and vitamin D". Артериосклероз, тромбоз и биология сосудов. 20 (2): 317–27. Дои:10.1161/01.ATV.20.2.317. PMID 10669626.
- ^ Geleijnse JM, Vermeer C, Grobbee DE, Schurgers LJ, Knapen MH, van der Meer IM, Hofman A, Witteman JC (November 2004). "Dietary intake of menaquinone is associated with a reduced risk of coronary heart disease: the Rotterdam Study". Журнал питания. 134 (11): 3100–5. Дои:10.1093/jn/134.11.3100. PMID 15514282.
- ^ "Linus Pauling Institute at Oregon State University". lpi.oregonstate.edu. В архиве from the original on 7 April 2010. Получено 2010-03-25.
- ^ «10 основных причин смерти». www.who.int. Получено 2020-01-26.
- ^ Pfuntner A, Wier LM, Steiner C (December 2013). "Costs for Hospital Stays in the United States, 2011". HCUP Statistical Brief #168. Роквилл, Мэриленд: Агентство медицинских исследований и качества.
- ^ Barter PJ, Caulfield M, Eriksson M, Grundy SM, Kastelein JJ, Komajda M, Lopez-Sendon J, Mosca L, Tardif JC, Waters DD, Shear CL, Revkin JH, Buhr KA, Fisher MR, Tall AR, Brewer B (November 2007). "Effects of torcetrapib in patients at high risk for coronary events". Медицинский журнал Новой Англии. 357 (21): 2109–22. Дои:10.1056/NEJMoa0706628. PMID 17984165.
- ^ Nilsson J, Hansson GK, Shah PK (January 2005). "Immunomodulation of atherosclerosis: implications for vaccine development". Артериосклероз, тромбоз и биология сосудов. 25 (1): 18–28. Дои:10.1161/01.ATV.0000149142.42590.a2. PMID 15514204.
- ^ Spiteller G (November 2005). "The relation of lipid peroxidation processes with atherogenesis: a new theory on atherogenesis". Молекулярное питание и пищевые исследования. 49 (11): 999–1013. Дои:10.1002/mnfr.200500055. PMID 16270286.
- ^ Berbée JF, Mol IM, Milne GL, Pollock E, Hoeke G, Lütjohann D, Monaco C, Rensen PC, van der Ploeg LH, Shchepinov MS (September 2017). "Deuterium-reinforced polyunsaturated fatty acids protect against atherosclerosis by lowering lipid peroxidation and hypercholesterolemia". Атеросклероз. 264: 100–107. Дои:10.1016/j.atherosclerosis.2017.06.916. PMID 28655430.
- ^ Tsikas D (September 2017). "Combating atherosclerosis with heavy PUFAs: Deuteron not proton is the first". Атеросклероз. 264: 79–82. Дои:10.1016/j.atherosclerosis.2017.07.018. PMID 28756876.
- ^ а б Chen WJ, Yin K, Zhao GJ, Fu YC, Tang CK (June 2012). "The magic and mystery of microRNA-27 in atherosclerosis". Атеросклероз. 222 (2): 314–23. Дои:10.1016/j.atherosclerosis.2012.01.020. PMID 22307089.
- ^ Sacco J, Adeli K (June 2012). "MicroRNAs: emerging roles in lipid and lipoprotein metabolism". Current Opinion in Lipidology. 23 (3): 220–5. Дои:10.1097/MOL.0b013e3283534c9f. PMID 22488426. S2CID 23814795.
- ^ Bommer GT, MacDougald OA (March 2011). "Regulation of lipid homeostasis by the bifunctional SREBF2-miR33a locus". Клеточный метаболизм. 13 (3): 241–7. Дои:10.1016/j.cmet.2011.02.004. ЧВК 3062104. PMID 21356514.
- ^ Rayner KJ, Sheedy FJ, Esau CC, Hussain FN, Temel RE, Parathath S, van Gils JM, Rayner AJ, Chang AN, Suarez Y, Fernandez-Hernando C, Fisher EA, Moore KJ (July 2011). "Antagonism of miR-33 in mice promotes reverse cholesterol transport and regression of atherosclerosis". Журнал клинических исследований. 121 (7): 2921–31. Дои:10.1172/JCI57275. ЧВК 3223840. PMID 21646721.
- ^ Iwakiri Y (March 2012). "A role of miR-33 for cell cycle progression and cell proliferation". Клеточный цикл. 11 (6): 1057–8. Дои:10.4161/cc.11.6.19744. PMID 22395363.
- ^ Singaraja RR, Stahmer B, Brundert M, Merkel M, Heeren J, Bissada N, Kang M, Timmins JM, Ramakrishnan R, Parks JS, Hayden MR, Rinninger F (August 2006). "Hepatic ATP-binding cassette transporter A1 is a key molecule in high-density lipoprotein cholesteryl ester metabolism in mice". Артериосклероз, тромбоз и биология сосудов. 26 (8): 1821–7. Дои:10.1161/01.ATV.0000229219.13757.a2. PMID 16728652.
- ^ Zimmer S, Grebe A, Bakke SS, Bode N, Halvorsen B, Ulas T, Skjelland M, De Nardo D, Labzin LI, Kerksiek A, Hempel C, Heneka MT, Hawxhurst V, Fitzgerald ML, Trebicka J, Björkhem I, Gustafsson JÅ, Westerterp M, Tall AR, Wright SD, Espevik T, Schultze JL, Nickenig G, Lütjohann D, Latz E (April 2016). «Циклодекстрин способствует регрессу атеросклероза через перепрограммирование макрофагов». Научная трансляционная медицина. 8 (333): 333ra50. Дои:10.1126 / scitranslmed.aad6100. ЧВК 4878149. PMID 27053774. Сложить резюме – Новости науки.
- ^ Wu H, Roks AJ (February 2014). "Genomic instability and vascular aging: a focus on nucleotide excision repair". Тенденции в сердечно-сосудистой медицине. 24 (2): 61–8. Дои:10.1016/j.tcm.2013.06.005. PMID 23953979.
- ^ а б Bautista-Niño PK, Portilla-Fernandez E, Vaughan DE, Danser AH, Roks AJ (May 2016). "DNA Damage: A Main Determinant of Vascular Aging". Международный журнал молекулярных наук. 17 (5): 748. Дои:10.3390/ijms17050748. ЧВК 4881569. PMID 27213333.
- ^ Shah AV, Bennett MR (December 2017). "DNA damage-dependent mechanisms of ageing and disease in the macro- and microvasculature". Европейский журнал фармакологии. 816: 116–128. Дои:10.1016/j.ejphar.2017.03.050. PMID 28347738. S2CID 1034518.
- ^ а б Martinet W, Knaapen MW, De Meyer GR, Herman AG, Kockx MM (August 2002). "Elevated levels of oxidative DNA damage and DNA repair enzymes in human atherosclerotic plaques". Тираж. 106 (8): 927–32. Дои:10.1161/01.cir.0000026393.47805.21. PMID 12186795.
- ^ Ishida T, Ishida M, Tashiro S, Yoshizumi M, Kihara Y (2014). "Role of DNA damage in cardiovascular disease". Тираж Журнал. 78 (1): 42–50. Дои:10.1253/circj.CJ-13-1194. PMID 24334614.
- ^ а б Barrington WT, Lusis AJ (December 2017). "Atherosclerosis: Association between the gut microbiome and atherosclerosis". Обзоры природы. Кардиология. 14 (12): 699–700. Дои:10.1038/nrcardio.2017.169. ЧВК 5815826. PMID 29099096.
- ^ Jie Z, Xia H, Zhong SL, Feng Q, Li S, Liang S, et al. (Октябрь 2017 г.). "The gut microbiome in atherosclerotic cardiovascular disease". Nature Communications. 8 (1): 845. Bibcode:2017NatCo...8..845J. Дои:10.1038/s41467-017-00900-1. ЧВК 5635030. PMID 29018189.
- ^ а б c Харман, Дженнифер Л .; Йоргенсен, Хелле Ф. (октябрь 2019 г.). «Роль гладкомышечных клеток в стабильности бляшек: терапевтический потенциал воздействия». Британский журнал фармакологии. 176 (19): 3741–3753. Дои:10.1111 / bph.14779. ISSN 0007-1188. ЧВК 6780045. PMID 31254285.
- ^ Bennett, Martin R.; Sinha, Sanjay; Owens, Gary K. (2016-02-19). "Vascular Smooth Muscle Cells in Atherosclerosis". Циркуляционные исследования. 118 (4): 692–702. Дои:10.1161 / CIRCRESAHA.115.306361. ISSN 0009-7330. ЧВК 4762053. PMID 26892967.
- ^ Gomez, Delphine; Shankman, Laura L; Nguyen, Anh T; Owens, Gary K (February 2013). "Detection of Histone Modifications at Specific Gene Loci in Single Cells in Histological Sections". Методы природы. 10 (2): 171–177. Дои:10.1038/nmeth.2332. ISSN 1548-7091. ЧВК 3560316. PMID 23314172.
- ^ Ван, Инь; Dubland, Joshua A.; Allahverdian, Sima; Asonye, Enyinnaya; Sahin, Basak; Jaw, Jen Erh; Sin, Don D.; Seidman, Michael A.; Leeper, Nicholas J.; Francis, Gordon A. (May 2019). "Smooth Muscle Cells Contribute the Majority of Foam Cells in ApoE (Apolipoprotein E)-Deficient Mouse Atherosclerosis". Артериосклероз, тромбоз и биология сосудов. 39 (5): 876–887. Дои:10.1161/ATVBAHA.119.312434. ISSN 1079-5642. ЧВК 6482082. PMID 30786740.
- ^ а б Chappell, Joel; Харман, Дженнифер Л .; Narasimhan, Vagheesh M .; Yu, Haixiang; Foote, Kirsty; Simons, Benjamin D.; Bennett, Martin R.; Jørgensen, Helle F. (2016-12-09). "Extensive Proliferation of a Subset of Differentiated, yet Plastic, Medial Vascular Smooth Muscle Cells Contributes to Neointimal Formation in Mouse Injury and Atherosclerosis Models". Циркуляционные исследования. 119 (12): 1313–1323. Дои:10.1161/CIRCRESAHA.116.309799. ISSN 0009-7330. ЧВК 5149073. PMID 27682618.
- ^ Durham, Andrew L; Speer, Mei Y; Scatena, Marta; Giachelli, Cecilia M; Shanahan, Catherine M (2018-03-15). "Role of smooth muscle cells in vascular calcification: implications in atherosclerosis and arterial stiffness". Сердечно-сосудистые исследования. 114 (4): 590–600. Дои:10.1093/cvr/cvy010. ISSN 0008-6363. ЧВК 5852633. PMID 29514202.
- ^ Basatemur, Gemma L.; Jørgensen, Helle F.; Clarke, Murray C. H.; Bennett, Martin R.; Mallat, Ziad (December 2019). «Клетки гладких мышц сосудов при атеросклерозе». Nature Reviews Кардиология. 16 (12): 727–744. Дои:10.1038/s41569-019-0227-9. ISSN 1759-5002. PMID 31243391. S2CID 195657448.
- ^ Ван, Инь; Dubland, Joshua A.; Allahverdian, Sima; Asonye, Enyinnaya; Sahin, Basak; Jaw, Jen Erh; Sin, Don D.; Seidman, Michael A.; Leeper, Nicholas J.; Francis, Gordon A. (May 2019). "Smooth Muscle Cells Contribute the Majority of Foam Cells in ApoE (Apolipoprotein E)-Deficient Mouse Atherosclerosis". Артериосклероз, тромбоз и биология сосудов. 39 (5): 876–887. Дои:10.1161/ATVBAHA.119.312434. ISSN 1079-5642. ЧВК 6482082. PMID 30786740.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |

